题目内容
下列实验设计及其对应离子方程式均正确的是( )
A.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+===Cu2++2Fe2+
B.Na2O2与H2O反应制备O2:Na2O2+H2O===2Na++2OH-+O2↑
C.将氯气溶于水制备次氯酸:Cl2+H2O===2H++Cl-+ClO-
D.用浓盐酸酸化的KMnO4与H2O2反应,证明H2O2具有还原性:2MnO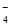 +6H++5H2O2===2Mn2++5O2↑+8H2O
+6H++5H2O2===2Mn2++5O2↑+8H2O
A
【解析】
试题分析:A、氯化铁与Cu反应生成氯化亚铁和氯化铜,所以用FeCl3溶液腐蚀铜线路板,设计合理且离子方程式正确;B、过氧化钠与水反应生成氢氧化钠和氧气,O元素不守恒,离子方程式错误;C、氯气与水反应生成氯化氢和次氯酸,但次氯酸是弱酸,不能拆开,所以离子方程式错误;D、浓盐酸酸化的高锰酸钾溶液中,高锰酸钾同样与氯离子反应生成氯气,实验设计不合理,错误,答案选A。
考点:考查对实验方案的评价及离子方程式书写的判断

练习册系列答案
相关题目
 乙
乙 丙
丙 甲,则甲不可能是
甲,则甲不可能是
 H分别是-285.8 kJ·mol-1、-283.0 kJ·mol-1和-726.5 kJ·mol-1。下列有关叙述正确的是
H分别是-285.8 kJ·mol-1、-283.0 kJ·mol-1和-726.5 kJ·mol-1。下列有关叙述正确的是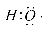 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同