题目内容
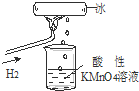 我校化学兴趣小组做了一个如图所示的实验,发现烧杯中酸性KMnO4溶液褪色.若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液显红色.则该条件下( )
我校化学兴趣小组做了一个如图所示的实验,发现烧杯中酸性KMnO4溶液褪色.若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液显红色.则该条件下( )| A、生成的水分子化学性质比较活泼 |
| B、H2燃烧生成了具有氧化性的物质 |
| C、H2被冷却为液态氢,液氢的水溶液具有还原性 |
| D、H2燃烧的产物中可能含有一定量的H2O2 |
考点:性质实验方案的设计
专题:
分析:实验控制的条件是,氢气在空气中燃烧,产物遇冰块冷凝滴入烧杯中.据紫色的KMnO4溶液具有强氧化性,若使其褪色,必定有还原性物质滴入杯中;使FeCl2、KSCN混合溶液变红,必定有氧化性物质将Fe2+氧化.从而确定这一冷凝产物既有氧化性又有还原性,应是过氧化氢.
解答:
解:A、烧杯中酸性KMnO4溶液褪色,说明H2燃烧的产物中可能有还原性物质,水的化学性质比较稳定,不具有该性质,故A错误;
B、烧杯中酸性KMnO4溶液褪色,说明H2燃烧的产物中可能有还原性物质,若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液呈血红色,说明有Fe3+生成,进而说明H2燃烧的产物中可能有氧化性物质,由此说明H2燃烧的产物中可能有还原性和氧化性的物质,故B错误;
C、实验结果表明氢气已经燃烧,被冷却的氢气不能使高锰酸钾褪色,故C错误;
D、H2O2具有氧化性与还原性,遇强氧化剂是表现还原性,遇较强的还原剂是表现氧化性,该条件下H2燃烧的产物中可能含有一定量的H2O2,故D正确.
故选:D.
B、烧杯中酸性KMnO4溶液褪色,说明H2燃烧的产物中可能有还原性物质,若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液呈血红色,说明有Fe3+生成,进而说明H2燃烧的产物中可能有氧化性物质,由此说明H2燃烧的产物中可能有还原性和氧化性的物质,故B错误;
C、实验结果表明氢气已经燃烧,被冷却的氢气不能使高锰酸钾褪色,故C错误;
D、H2O2具有氧化性与还原性,遇强氧化剂是表现还原性,遇较强的还原剂是表现氧化性,该条件下H2燃烧的产物中可能含有一定量的H2O2,故D正确.
故选:D.
点评:本题考查化学实验现象的分析、物质的性质知识、氧化性与还原性等,难度不大,根据现象推断物质具有的性质是关键.

练习册系列答案
相关题目
下列说法中正确的是( )
| A、1 mol任何纯净物都含有相同的分子数 |
| B、1 mol氦气中约含有6.02×1023个氦原子 |
| C、1 mol水中含有8mol电子 |
| D、1 molNa的质量为23 g?mol-1 |
列物质按纯净物、混合物、电解质、非电解质的顺序组合正确的是( )
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | 硫酸 | 铜 |
| B | 胆矾 | 石灰水 | 硫酸钡 | NH3 |
| C | 火碱 | 蔗糖溶液 | 氯化钠溶液 | 三氧化硫 |
| D | 纯醋酸 | 氢氧化铁胶体 | 苛性钾溶液 | 乙醇 |
| A、A | B、B | C、C | D、D |
下列实验目的不能实现的是( )
A、 吸收氨气防倒吸 |
B、 实验室制硝基苯 |
C、 提纯工业乙醇 |
D、 分离苯和溴苯 |
下列实验仪器中,常用于物质分离的是( )
①容量瓶 ②漏斗 ③量筒 ④蒸馏烧瓶 ⑤分液漏斗 ⑥胶头滴管.
①容量瓶 ②漏斗 ③量筒 ④蒸馏烧瓶 ⑤分液漏斗 ⑥胶头滴管.
| A、①③⑤ | B、②④⑤ |
| C、③④⑥ | D、①②⑥ |