题目内容
14.化合物A、B和C互为同分异构体,它们的元素分析数据为:碳92.3%,氢7.7%,1molA在氧气中充分燃烧产生179.2L二氧化碳(标准状况).A是芳香族化合物,分子中所有的原子共平面,B是具有两个支链的链状化合物,核磁共振氢谱显示其有两种峰,且峰面积之比为3:1;C的一氯代物没有同分异构现象,而二氯代物却有三种同分异构体,且分子中只有碳碳单键和碳氢键.(1)写出A、B和C的分子式为:C8H8
(2)写出A、B和C的结构简式.
分析 (1)根据C、H元素的质量分数计算出最简式,然后根据碳原子守恒计算出A、B、C的分子式;
(2)A是芳香烃,分子式为C8H8的不饱和度为:$\frac{8×2+2-8}{2}$=5,其中苯环的不饱和度为4,则A中还含有1个碳碳双键,又由于A分子中所有的原子共平面,结合苯为平面结构、乙烯所有原子共平面可知A为苯乙烯;
B是具有两个支链的链状化合物,核磁共振氢谱显示其有两种峰,且峰面积之比为3:1,且B的不饱和度为:$\frac{8×2+2-8}{2}$=5,则B分子中应该含有2个碳碳三键和1个碳碳三键,据此确定B的结构简式;
C的一氯代物没有同分异构现象,而二氯代物却有三种同分异构体,且分子中只有碳碳单键和碳氢键,则C分子中碳原子的化学环境完全相同,应该为立方烷.
解答 解:(1)A、B、C分子中C、H原子数之比为:N(C):N(H)=$\frac{92.3%}{12}$:$\frac{7.7%}{1}$=1:1,则最简式为:CH,
设分子式为:CnHn,n=$\frac{179.2L}{22.4L/mol}$=8,故A、B、C的分子式为:C8H8;
故答案为:C8H8;
(2)A是芳香烃,分子式为C8H8的不饱和度为:$\frac{8×2+2-8}{2}$=5,其中苯环的不饱和度为4,则A中还含有1个碳碳双键,又由于A分子中所有的原子共平面,结合苯为平面结构、乙烯所有原子共平面可知A为苯乙烯,结构简式为 ;
;
B是具有两个支链的链状化合物,核磁共振氢谱显示其有两种峰,且峰面积之比为3:1,且B的不饱和度为:$\frac{8×2+2-8}{2}$=5,则B分子中应该含有2个碳碳三键和1个碳碳三键,则B的结构简式为:HC≡C-C(CH3)=C(CH3)-C≡CH;
C的一氯代物没有同分异构现象,而二氯代物却有三种同分异构体,且分子中只有碳碳单键和碳氢键,则C分子中碳原子的化学环境完全相同,应该为立方烷: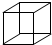 ,
,
答:A、B和C的结构简式分别为 、HC≡C-C(CH3)=C(CH3)-C≡CH、
、HC≡C-C(CH3)=C(CH3)-C≡CH、 .
.
点评 本题考查了有机物分子式、结构简式的确定,题目难度中等,明确常见有机物结构与性质为解答关键,推断B的结构简式为难点,注意掌握确定有机物结构简式的方法,试题培养了学生的分析能力及逻辑推理能力.

| A. | SO2的摩尔质量是64 g/mol | |
| B. | 常温常压下,64 g SO2中所含的原子数为3×6.02×1023 个 | |
| C. | 1 mol SO3的质量是80 g | |
| D. | 标准状况下,1 mol SO3的体积为22.4 L |
| A. | 1:2 | B. | 2:1 | C. | 2:3 | D. | 1:1 |
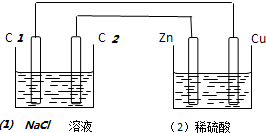
| A. | (1)中C2电极反应式为:2Cl--2e-═Cl2 | B. | (2)溶液中的SO42-向Cu极定向移动 | ||
| C. | (1)中滴入酚酞试液,C1极附近先变红 | D. | (2)中溶液的PH=1 |
| A. | ①②③ | B. | ①③④ | C. | ②③④ | D. | ①②③④ |
| A. | 5:1 | B. | 1:5 | C. | 5:9 | D. | 9:5 |
| A. | HClO是弱酸,所以NaClO是弱电解质 | |
| B. | BaO2是离子化合物,但含有非极性共价键,晶体中阴阳离子个数相等. | |
| C. | HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 | |
| D. | 电解NaCl溶液得到22.4LH2(标准状况),理论上需要转移NA个电子(NA表示阿伏加德罗常数) |

 ;C分子中的官能团有醚键和溴原子.(填名称)
;C分子中的官能团有醚键和溴原子.(填名称)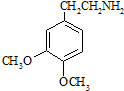 .
. .
.