题目内容
14.在标有“20℃,25mL”的滴定管内装酸液至刻度“0”时,管内液体的体积( )| A. | 大于25mL | B. | 等于25mL | C. | 小于25mL | D. | 无法判断 |
分析 滴定管的“0”刻度在上、满刻度在下(量筒与此相反),在刻度以下还有一段空间没有刻度.
解答 解:滴定管的“0”刻度在上、满刻度在下(量筒与此相反),在刻度以下还有一段空间没有刻度.因此,在标有“20℃,25mL”的滴定管内装溶液至刻度“0”时,管内液体的体积总量大于25mL,
故选A.
点评 本题考查滴定管的结构,题目难度不大,注意滴定管的“0”刻度在上、满刻度在下(量筒与此相反),满刻度以下还有一段空间没有刻度.

练习册系列答案
相关题目
4. 在狗年里,人们相互祝愿亲朋好友:狗年旺旺,狗年大发.图是一种形状酷似一条小狗的有机物键线式结构图,化学家将其取名为“doggycene”,下列有关“doggycene”的说法中正确的是( )
在狗年里,人们相互祝愿亲朋好友:狗年旺旺,狗年大发.图是一种形状酷似一条小狗的有机物键线式结构图,化学家将其取名为“doggycene”,下列有关“doggycene”的说法中正确的是( )
 在狗年里,人们相互祝愿亲朋好友:狗年旺旺,狗年大发.图是一种形状酷似一条小狗的有机物键线式结构图,化学家将其取名为“doggycene”,下列有关“doggycene”的说法中正确的是( )
在狗年里,人们相互祝愿亲朋好友:狗年旺旺,狗年大发.图是一种形状酷似一条小狗的有机物键线式结构图,化学家将其取名为“doggycene”,下列有关“doggycene”的说法中正确的是( )| A. | 该分子中所有碳原子不可能处于同一平面 | |
| B. | “doggycene”的分子式为C26H30 | |
| C. | 该物质在常温下呈气态 | |
| D. | 1 mol该物质在氧气中完全燃烧生成CO2和H2O的物质的量之比为1:1 |
2.判断溶液为中性的依据是( )
| A. | c(OH-)=1×10-7mol/L | B. | c(H+)=1×10-7mol/L | ||
| C. | c(OH-)=c(H+) | D. | pH=7 |
19.100mL 2.0 mol•L-1 的碳酸钠溶液和200mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,最终都有气体产生,但生成的气体体积不同,下列选项中盐酸的浓度合理的是( )
| A. | 2.0 mol•L-1 | B. | 1.5 mol•L-1 | C. | 1 mol•L-1 | D. | 0.5 mol•L-1 |
5.表为各物质中所含少量杂质以及除去这些杂质所选用的试剂或操作方法,正确的一组是( )
| 号序 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
| ① | KNO3 | KOH | 加入FeCl3溶液,并过滤 |
| ② | FeSO4 | CuSO4 | 加入足量铁粉后过滤 |
| ③ | O2 | CO2 | 依次通过盛有浓硫酸和NaOH溶液的洗气瓶 |
| ④ | CaO | CaCO3 | 加入稀盐酸,再蒸发 |
| A. | ①④ | B. | ② | C. | ②④ | D. | ②③ |
2.下列有关溶液组成的描述合理的是( )
| A. | 弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3- | |
| B. | 滴加石蕊呈红色的溶液可能大量存在K+、NH4+、Cl-、S2- | |
| C. | 与Al反应能放出H2的溶液中可能大量存在:Fe2+、K+、NO3-、SO42- | |
| D. | 漂白粉的水溶液可能大量存在Fe2+、Cl-、Ca2+、Na+ |
3.如图是利用废铜屑(含杂质)制备胆矾(硫酸铜晶体)的过程
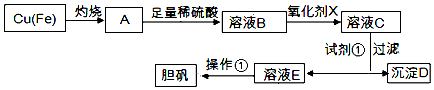
已知:
请回答:
(1)下列物质中最适宜做氧化剂X的是B(填字母).
A.NaClO B.H2O2 C.KMnO4 D.FeCl3
(2)加入试剂①是为了调节pH,试剂①可以选择CuO或CuCO3或Cu(OH)2(填化学式).
(3)操作①的名称是蒸发浓缩、冷却结晶.
(4)沉淀D加入盐酸可以得到FeCl3溶液,关于FeCl3溶液的性质中说法不正确的是C.
A.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
B.向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
C.将FeCl3溶液滴加NaOH溶液,将沉淀干燥灼烧,得到Fe(OH)3固体
D.向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(5)沉淀D加入盐酸和铁粉,可以制得FeCl2溶液,实验室保存FeCl2溶液,需加入过量的铁粉防止FeCl2溶液变质,其原因是Fe+2Fe3+=3Fe2+(用离子方程式表示).
(6)若用碳电极电解硫酸铜溶液200mL.通电5min后,阴极增重0.64g,则电解后溶液的pH=1(溶液体积变化忽略不计).

已知:
| 溶液中被沉淀的离子 | Fe3+ | Fe2+ | Cu2+ |
| 完全生成氢氧化物的沉淀时,溶液的pH | ≥3.7 | ≥6.4 | ≥4.4 |
(1)下列物质中最适宜做氧化剂X的是B(填字母).
A.NaClO B.H2O2 C.KMnO4 D.FeCl3
(2)加入试剂①是为了调节pH,试剂①可以选择CuO或CuCO3或Cu(OH)2(填化学式).
(3)操作①的名称是蒸发浓缩、冷却结晶.
(4)沉淀D加入盐酸可以得到FeCl3溶液,关于FeCl3溶液的性质中说法不正确的是C.
A.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
B.向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
C.将FeCl3溶液滴加NaOH溶液,将沉淀干燥灼烧,得到Fe(OH)3固体
D.向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(5)沉淀D加入盐酸和铁粉,可以制得FeCl2溶液,实验室保存FeCl2溶液,需加入过量的铁粉防止FeCl2溶液变质,其原因是Fe+2Fe3+=3Fe2+(用离子方程式表示).
(6)若用碳电极电解硫酸铜溶液200mL.通电5min后,阴极增重0.64g,则电解后溶液的pH=1(溶液体积变化忽略不计).
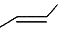 .有机物X的键线式为
.有机物X的键线式为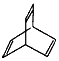
 .
.