题目内容
10.N2H4是一种高效清洁的火箭燃料.0.25mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5kJ热量.则下列热化学方程式中正确的是( )| A. | $\frac{1}{2}$N2H4(g)+$\frac{1}{2}$O2(g)═$\frac{1}{2}$N2(g)+H2O(l)△H=-267 kJ•mol-1 | |
| B. | N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-133.5 kJ•mol-1 | |
| C. | N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=+534 kJ•mol-1 | |
| D. | N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534 kJ•mol-1 |
分析 0.25mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5kJ热量,可知1molN2H4(g)完全燃烧生成氮气和气态水时,放出热量为$\frac{133.5kJ}{0.25}$=534kJ,焓变为负,结合热化学方程式中物质状态、n与热量成正比及焓变来解答.
解答 解:0.25mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5kJ热量,可知1molN2H4(g)完全燃烧生成氮气和气态水时,放出热量为$\frac{133.5kJ}{0.25}$=534kJ,焓变为负,则热化学方程式为N2H4(g)+O2(g)═N2(g)+2H2O(l)△H=-534 kJ•mol-1,
0.5mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5kJ×2=267kJ热量,热化学方程式为$\frac{1}{2}$N2H4(g)+$\frac{1}{2}$O2(g)═$\frac{1}{2}$N2(g)+H2O(l)△H=-267 kJ•mol-1,
故选A.
点评 本题考查热化学方程式的书写,为高频考点,把握热化学方程式的书写方法、物质的量与热量的关系为解答的关键,侧重分析与应用能力的考查,注意焓变为负及水的状态,题目难度不大.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案
相关题目
1.氢气是一种清洁能源.科学家探究太阳能制氢技术,设计流程图如图1:

信息提示:以下反应均在150℃发生
2HI(aq)?H2(g)+I2(g )△H1
SO2(g)+I2(g)+2H2O(g)=H2SO4(l)+2HI(g)△H2
2H2SO4(l)?2H2O(g)+2SO2(g)+O2(g)△H3
2H2O(g)=2H2(g)+O2(g)△H4
请回答下列问题:
(1)△H4与△H1、△H2、△H3之间的关系是:△H4=2△H1+2△H2+△H3.
(2)该制氢气技术的优点是物质循环利用,能源来自太阳能,无污染且取之不尽用之不竭(两个要点,一个是物质循环、一个是能量),若反应SO2(g)+I2(g)+2H2O(g)=H2SO4(l)+2HI(g)在150℃下能自发进行,则△H<0(填“>”,“<”或“=”).
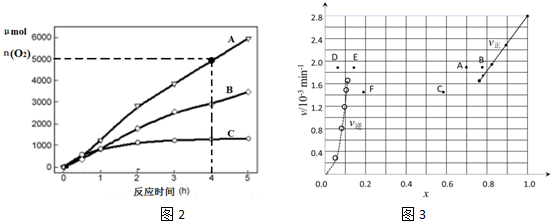
(3)在某温度下,H2SO4在不同催化剂条件下分解产生氧气的量随时间变化如图2所示.则下列说法正确的是BD.
A.H2SO4分解反应的活化能大小顺序是:Ea(A)>Ea( B )>Ea(C )
B.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明该反应已经达到平衡
C.0~4小时在A催化剂作用下,H2SO4分解的平均速率v(O2)=1250mol•h-1
D.不同催化剂的催化效果不同,是因为活化分子百分数不相同
(4)对于反应:2HI(g)?H2(g)+I2(g),在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
①根据上述实验结果,该反应的平衡常数K的计算式为:$K=\frac{0.108×0.108}{{{{0.784}^2}}}$.
②上述反应中,正反应速率为v正=k正•x2(HI),逆反应速率为v逆=k逆•x(H2)•x(I2),其中k正、k逆为速率常数,则k逆为k逆=$\frac{K正}{K}$(以K和k正表示).若k正=0.0027min-1,在t=40min时,v正=1.95×10-3min-1
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用图3表示.当升高到某一温度时,反应重新达到平衡,相应的点分别为A、E(填字母)

信息提示:以下反应均在150℃发生
2HI(aq)?H2(g)+I2(g )△H1
SO2(g)+I2(g)+2H2O(g)=H2SO4(l)+2HI(g)△H2
2H2SO4(l)?2H2O(g)+2SO2(g)+O2(g)△H3
2H2O(g)=2H2(g)+O2(g)△H4
请回答下列问题:
(1)△H4与△H1、△H2、△H3之间的关系是:△H4=2△H1+2△H2+△H3.
(2)该制氢气技术的优点是物质循环利用,能源来自太阳能,无污染且取之不尽用之不竭(两个要点,一个是物质循环、一个是能量),若反应SO2(g)+I2(g)+2H2O(g)=H2SO4(l)+2HI(g)在150℃下能自发进行,则△H<0(填“>”,“<”或“=”).
(3)在某温度下,H2SO4在不同催化剂条件下分解产生氧气的量随时间变化如图2所示.则下列说法正确的是BD.
A.H2SO4分解反应的活化能大小顺序是:Ea(A)>Ea( B )>Ea(C )
B.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明该反应已经达到平衡
C.0~4小时在A催化剂作用下,H2SO4分解的平均速率v(O2)=1250mol•h-1
D.不同催化剂的催化效果不同,是因为活化分子百分数不相同
(4)对于反应:2HI(g)?H2(g)+I2(g),在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
②上述反应中,正反应速率为v正=k正•x2(HI),逆反应速率为v逆=k逆•x(H2)•x(I2),其中k正、k逆为速率常数,则k逆为k逆=$\frac{K正}{K}$(以K和k正表示).若k正=0.0027min-1,在t=40min时,v正=1.95×10-3min-1
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用图3表示.当升高到某一温度时,反应重新达到平衡,相应的点分别为A、E(填字母)

15.常温下,下列各组数据中比值为2:1的是( )
| A. | 熔融NaHSO4电离出的阳离子与阴离子之比 | |
| B. | 0.2mol•L-1的CH3COOH溶液与0.1mol•L-1的盐酸中c(H+)之比 | |
| C. | pH=7的氨水与(NH4)2SO4的混合溶液中,c(NH4+)与c(SO42-)之比 | |
| D. | pH=12的Ba(OH)2溶液与pH=12的KOH溶液中c(OH-)之比 |
 H++In-(黄色),对上述平衡解释不正确的是
H++In-(黄色),对上述平衡解释不正确的是 
 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.