题目内容
3.如图所示,一密闭容器被无摩擦、可滑动的两隔板a、b分成甲、乙两室;标准状况下,在乙室中充入0.4mol HCl,甲室中充入NH3、H2的混合气体,静止时活塞位置如图.已知甲、乙两室中气体的质量之差为7.0g.
(1)甲室中气体的物质的量为0.8mol.
(2)甲室中NH3,H2的物质的量之比为1:1.
(3)将隔板a去掉,当HCl与NH3充分反应生成NH4Cl固体后,活塞b将位于刻度“2”处(填数字,不考虑固体物质产生的压强).
分析 (1)相同条件下,气体的物质的量之比等于其体积之比;
(2)根据甲室中气体的物质的量和质量计算氨气和氢气的物质的量之比、质量之比;
(3)根据剩余气体的物质的量计算剩余气体所占体积,从而确定b的位置.
解答 解:(1)相同条件下,气体的物质的量之比等于其体积之比,看图可知甲、乙两室气体的体积比为2:1,故其物质的量之比为2:1,在乙室中充入0.4mol HCl,所以甲室中气体为0.8mol,
故答案为:0.8mol;
(2)0.4mol HCl的质量为0.4mol×36.5g/mol=14.6g,甲、乙两室中气体的质量之差为7.0g,则甲中气体为7.6g,
设氨气的物质的量为x,氢气的物质的量为y,
根据其物质的量、质量列方程组为:$\left\{\begin{array}{l}{x+y=0.8}\\{17x+2y=7.6}\end{array}\right.$,解得x=0.4mol,y=0.4mol,所以氨气和氢气的物质的量之比0.4mol:0.4mol=1:1,
故答案为:1:1;
(3)甲室中NH3的物质的量为0.4mol,恰好等于HCl的物质的量,所以二者恰好完全反应生成NH4Cl固体,剩余H2的物质的量为0.4mol,相同条件下,气体的体积之比等于其物质的量之比,所以活塞b将会左移至“2”处,故答案为:2.
点评 本题考查物质的量及浓度的计算,为高频考点,把握物质的量为中心的基本计算公式及明确相同条件下气体的体积之比等于物质的量之比为解答的关键,侧重分析与计算能力的考查,题目难度不大.

| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O | |
| B. | 向Na2SiO3溶液中通入过量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| C. | 向Al2(SO4)3溶液中加入过量的NH3•H2O:Al3++4 NH3•H2O═AlO2-+4NH4+ | |
| D. | 向CuSO4溶液中加入Na:2 Na+Cu2++2H2O═2Na++Cu(OH)2↓+H2↑ |
 一块表面被氧化的铝分成两等分,若向其中一份中滴加1mol•L-1的NaOH溶液,向另一份中滴加x mol•L-1的稀盐酸,产生氢气的物质的量与所加NaOH溶液、稀盐酸的体积关系如图所示.下列说法不正确的是( )
一块表面被氧化的铝分成两等分,若向其中一份中滴加1mol•L-1的NaOH溶液,向另一份中滴加x mol•L-1的稀盐酸,产生氢气的物质的量与所加NaOH溶液、稀盐酸的体积关系如图所示.下列说法不正确的是( )| A. | 该铝块的总质量为8.46g | |
| B. | a=260 | |
| C. | b=780 | |
| D. | 该铝块中氧化铝与铝单质的物质的量之比为3:20 |
| A. | -83.6kJ/mol | B. | -26.3kJ/mol | C. | 26.3kJ/mol | D. | 83.6kJ/mol |
| A. | 乙烯 | B. | 丙烯 | C. | 2-甲基丙烯 | D. | 2-丁烯 |
实验室里需要配制480mL 0.10mol·L-1的硫酸铜溶液,下列实验方案及实验操作正确的是
选项 | 容量瓶容积 | 溶质质量 | 实验操作 |
A | 480mL | 硫酸铜:7.68g | 加入 500mL水 |
B | 480mL | 胆矾:12.0g | 配成500mL溶液 |
C | 500mL | 硫酸铜:8.0g | 加入500mL水 |
D | 500mL | 胆矾:12.5g | 配成500mL溶液 |
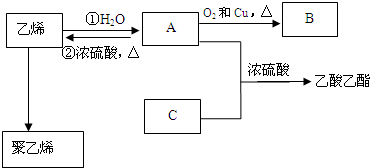
 ,化合物C所含官能团的名称为羧基.
,化合物C所含官能团的名称为羧基. $→_{△}^{浓硫酸}$R-CH=CH2+H2O,写出反应②的反应方程式(标明反应条件):CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$H2O+CH2=CH2↑.
$→_{△}^{浓硫酸}$R-CH=CH2+H2O,写出反应②的反应方程式(标明反应条件):CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$H2O+CH2=CH2↑. 据2006年11月12 中央电视台每周质量报告报道,北京市场上销售的一部分标称是白洋淀特产的“红心鸭蛋”含偶氮染料“苏丹红Ⅳ号”,国际癌症研究机构将其列为三类致癌物.
据2006年11月12 中央电视台每周质量报告报道,北京市场上销售的一部分标称是白洋淀特产的“红心鸭蛋”含偶氮染料“苏丹红Ⅳ号”,国际癌症研究机构将其列为三类致癌物. 空间结构,且是不能旋转不然,双键就会被破坏,而单键是可以旋转的,则肯定共线的原子最多有12个.
空间结构,且是不能旋转不然,双键就会被破坏,而单键是可以旋转的,则肯定共线的原子最多有12个.