题目内容
8.已知H2SO4(aq)与Ba(OH)2(aq)反应的△H=-140.9kJ/mol;HCl(aq)与NaOH(aq)反应的△H=-57.3kJ/mol,则生成BaSO4(s)的反应热等于( )| A. | -83.6kJ/mol | B. | -26.3kJ/mol | C. | 26.3kJ/mol | D. | 83.6kJ/mol |
分析 分别写出写出稀硫酸与氢氧化钡溶液、氢离子与氢氧根离子反应的热化学方程式,然后利用盖斯定律计算出钡离子与硫酸根离子反应生成硫酸钡的反应热.
解答 解:硫酸雨氢氧化钡的反应为:①2H+(aq)+SO42-(aq)+Ba2+(aq)+2OH-(aq)=BaSO4↓(s)+2H2O(l)△H=-140.9 kJ•mol-1,
HCl(aq)与NaOH(aq)反应的△H=-57.3kJ/mol,则②H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ•mol-1,
生成硫酸钡沉淀的反应为:③SO42-(aq)+Ba2+(aq)=BaSO4↓(s)△H,
根据盖斯定律,①-②×2可得:SO42-(aq)+Ba2+(aq)=BaSO4↓(s)△H=(-140.9 kJ•mol-1)-(-57.3 kJ•mol-1)×2=-26.3kJ/mol,
故选B.
点评 本题考查了热化学方程的计算,题目难度中等,明确盖斯定律的含义为解答关键,注意掌握热化学方程式的书写原则,试题培养了学生的灵活运用能力.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
2. 已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )
已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )
 已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )
已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )| A. | 加入催化剂,减小了反应的热效应 | |
| B. | 加入催化剂,可提高H2O2的平衡转化率 | |
| C. | 反应物的总能量高于生成物的总能量 | |
| D. | H2O2分解的热化学方程式:H2O2═H2O+$\frac{1}{2}$O2△H<0 |
19.在某温度下,反应ClF(g)+F2(g)?ClF3(g)(正反应为放热反应)在密闭容器中达到平衡.下列说法正确的是( )
| A. | 温度不变,缩小体积,ClF的转化率减小 | |
| B. | 温度不变,增大体积,ClF3的产率提高 | |
| C. | 升高温度,增大体积,平衡向正反应方向移动 | |
| D. | 降低温度,体积不变,F2的转化率升高 |
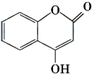 可用来制备抗凝血药,通过如图路线合成:
可用来制备抗凝血药,通过如图路线合成: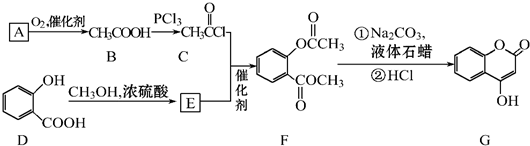
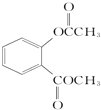 +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$ +CH3COONa+CH3OH+H2O.
+CH3COONa+CH3OH+H2O.