题目内容
一定条件下,氨气和氟气可以发生反应:4NH3+3F2→NF3+3NH4F,其中NF3分子空间构型与NH3相似.下列说法错误的是( )
| A、NF3是由极性键构成的极性分子 |
| B、氧化产物只有NF3,还原产物有NF3和NH4F |
| C、4 mol NH3被氧化时转移电子的物质的量为6 mol |
| D、NH4F属于离子晶体,既含有离子键又含有共价键 |
考点:氧化还原反应,化学键
专题:氧化还原反应专题
分析:A、分子结构对称,正负电荷中心重叠,则为非极性分子;
B、根据化合价的变化判断;
C、根据NH3中N元素的化合价的变化判断;
D、根据NH4Cl化学键类型判断NH4F的化学键类型;
B、根据化合价的变化判断;
C、根据NH3中N元素的化合价的变化判断;
D、根据NH4Cl化学键类型判断NH4F的化学键类型;
解答:
解:A、NF3分子构型与NH3相似,NH3分子构型是三角锥型的,所以NF3分子构型也是三角锥型的,三角锥形分子的结构不对称,正负电荷中心不重叠,为极性分子,故A正确;
B、NH3反应中N元素的化合价升高被氧化,F2中F元素的化合价降低被还原,则氧化产物只有NF3,还原产物有NF3和NH4F,故B正确;
C、NH3被氧化时N元素的化合价有-3价升高到+3价失去6个电子,则4 mol NH3被氧化时转移电子的物质的量为24 mol,故C错误;
D、NH4Cl与NH4F含的阳离子相同,阴离子是同一主族元素,所以NH4Cl与NH4F具有相同的化学键,所以NH4F中存在的化学键是离子键、极性共价键,故D正确;
故选C.
B、NH3反应中N元素的化合价升高被氧化,F2中F元素的化合价降低被还原,则氧化产物只有NF3,还原产物有NF3和NH4F,故B正确;
C、NH3被氧化时N元素的化合价有-3价升高到+3价失去6个电子,则4 mol NH3被氧化时转移电子的物质的量为24 mol,故C错误;
D、NH4Cl与NH4F含的阳离子相同,阴离子是同一主族元素,所以NH4Cl与NH4F具有相同的化学键,所以NH4F中存在的化学键是离子键、极性共价键,故D正确;
故选C.
点评:本题考查物质的结构、化学键、物质的分类、氧化还原反应,该反应中元素的化合价的判断是解答的关键,并注意类推方法的应用.

练习册系列答案
相关题目
某种由Na2S、Na2SO3、Na2SO4组成的固体混合物中,已知S的质量分数为25.6%,则氧的质量分数为( )
| A、51.2% | B、36.8% |
| C、37.6% | D、无法计算 |
 已知:X、Y、Z、W为短周期元素,原子半径X:99pm Y:154pm Z:125pm W:117pm,X Y W位置如图所示(副族省略),X、Y、Z的最高价氧化物对应的水化物相互能反应,下列说法正确的是( )
已知:X、Y、Z、W为短周期元素,原子半径X:99pm Y:154pm Z:125pm W:117pm,X Y W位置如图所示(副族省略),X、Y、Z的最高价氧化物对应的水化物相互能反应,下列说法正确的是( )| A、元素Z处于周期表的阴影位置 |
| B、非金属性:X>W |
| C、X与W形成化合物熔点很高,为离子化合物 |
| D、Y、W的最高价氧化物对应的水化物能反应 |
下列化合物分别与金属钠反应,其中反应最慢的是( )
| A、CH3CH2OH |
| B、CH3COOH |
| C、H2O |
| D、C6H5OH |
下列物质既能与盐酸反应又能与氢氧化钠溶液反应的是( )
①Al②Al2O3③Al(OH3)④Fe.
①Al②Al2O3③Al(OH3)④Fe.
| A、① | B、①② |
| C、①②③ | D、①②③④ |
下列各项操作中不发生先沉淀后溶解现象的是( )
①向饱和碳酸钠溶液中通入过量的CO2
②向Fe(OH)3胶体中逐滴加入过量H2SO4
③向Ba(NO3)2溶液中通入过量SO3
④向石灰水中通入过量CO2
⑤向硅酸钠溶液中逐滴加入过量的盐酸.
①向饱和碳酸钠溶液中通入过量的CO2
②向Fe(OH)3胶体中逐滴加入过量H2SO4
③向Ba(NO3)2溶液中通入过量SO3
④向石灰水中通入过量CO2
⑤向硅酸钠溶液中逐滴加入过量的盐酸.
| A、①②③ | B、①②⑤ |
| C、①②③⑤ | D、①③⑤ |
铝能用于冶炼金属铁、钒、铬、锰等,其原因是铝具有( )
| A、两性 |
| B、导电性好 |
| C、熔点低 |
| D、还原性强,且反应放出大量热 |

 .
.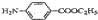 )的合成路线流程图(必要条件需注明,无机试剂任选).合成路线流程图示例如下:
)的合成路线流程图(必要条件需注明,无机试剂任选).合成路线流程图示例如下: