题目内容
5.下列实验能获得成功的是( )| A. | 将苯逐滴滴入浓硝酸和稀硫酸的混合液中,并用沸水浴加热制取硝基苯 | |
| B. | 油脂的提纯中,可将油脂加入浓NaOH 溶液加热,然后过滤,从滤液中可得较纯的油脂 | |
| C. | 将铜丝在酒精灯上加热到红热后,立即伸入无水乙醇中,反复操作多次,可制得乙醛 | |
| D. | 淀粉用酸催化水解后的溶液加入银氨溶液,水浴加热,可看到有银镜出现 |
分析 A.硝基苯制取时需要55-60℃;
B.油脂是高级脂肪酸甘油酯,碱性条件下易水解;
C.在Cu作催化剂、加热条件下,乙醇被氧化生成乙醛;
D.淀粉水解后的溶液做银镜反应时应该先加氢氧化钠中和酸.
解答 解:A.硝基苯制取时需要55-60℃,应该用水浴加热,故A错误;
B.油脂是高级脂肪酸甘油酯,在碱性条件下能发生水解生成,高级脂肪酸和甘油,故B错误;
C.在Cu作催化剂、加热条件下,乙醇被氧化生成乙醛,所以将铜丝在酒精灯上加热到红热后,立即伸入无水乙醇中,反复操作多次,可制得乙醛,故C正确;
D.淀粉水解后的溶液做银镜反应时应该先加氢氧化钠中和酸,银镜反应必须在碱性条件下进行,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及实验基本操作、实验原理等知识点,明确实验原理及实验操作规范性是解本题关键,注意D中反应必须在碱性条件下,为易错点.

练习册系列答案
相关题目
15.25℃、101kPa下,4g CH4完全燃烧生成CO2和液态水时,放出222.5kJ的热量,则下列热化学方程式中正确的是( )
| A. | CH4(g)+2O2(g)═CO2(g)+2 H2O(g )△H=-890kJ/mol | |
| B. | CH4(g)+2O2(g)═CO2(g)+2 H2O(l )△H=+890kJ/mol | |
| C. | $\frac{1}{2}$CH4(g)+O2(g)═$\frac{1}{2}$CO2(g)+H2O(1)△H=-445kJ/mol | |
| D. | CH4(g)+2O2(g)═CO2(g)+2 H2O(l )△H=-890kJ |
16.用石墨作电极,电解1mol/L下列物质的溶液,则电解前后溶液的pH保持不变的是( )
| A. | HCl | B. | NaOH | C. | CuSO4 | D. | KNO3 |
20.常温下均不溶于水且比水轻的一组液体是( )
| A. | 溴苯 乙酸 | B. | 硝基苯 氯乙烷 | C. | 甲苯 乙酸乙酯 | D. | 苯 乙醇 |
10.现有A、B两种有机物,无论以何种比例混合,只要混合物总质量一定,完全燃烧后,生成的H2O的质量也一定.下列结论正确的是( )
| A. | A、B中的氢的质量分数必相等 | |
| B. | A、B的实验式必相同 | |
| C. | A、B一定是同系物 | |
| D. | A、B可以是烃,也可以是烃的含氧衍生物 |
10.氢气是一种清洁能源.用甲烷制取氢气的两步反应的能量变化如下图所示:
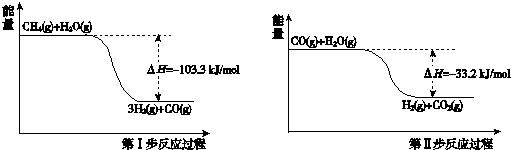
(1)甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是CH4(g)+2H2O(g)=4H2(g)+CO2(g)△H=-136.5kJ/mol.
(2)第II步为可逆反应.在800℃时,若CO的起始浓度为2.0mol/L,水蒸气的起始浓度为3.0mol/L,达到化学平衡状态后,测得CO2的浓度为1.2mol/L,则此反应的平衡常数为1,随着温度升高该反应的化学平衡常数的变化趋势是变小.
(3)在恒温恒容密闭容器中进行的第II步反应,下列说法中能表示达到平衡状态的是bc(填序号).
a.四种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比
b.单位时间内断开amol H-H键的同时断开2a mol O-H键
c.反应容器中放出的热量不再变化
d.混合气体的密度不再发生变化
e.混合气体的压强不再发生变化
(4)某温度下,第Ⅱ步反应的平衡常数为K=$\frac{1}{9}$.该温度下在甲、乙、丙三个恒容密闭容器中投入H2O(g)和CO(g),其起始浓度如下表所示.下列判断不正确的是CD.
A.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
B.平衡时,甲中和丙中H2O的转化率均是25%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.015mol/L
D.平衡时,乙中H2O的转化率大于25%

(1)甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是CH4(g)+2H2O(g)=4H2(g)+CO2(g)△H=-136.5kJ/mol.
(2)第II步为可逆反应.在800℃时,若CO的起始浓度为2.0mol/L,水蒸气的起始浓度为3.0mol/L,达到化学平衡状态后,测得CO2的浓度为1.2mol/L,则此反应的平衡常数为1,随着温度升高该反应的化学平衡常数的变化趋势是变小.
(3)在恒温恒容密闭容器中进行的第II步反应,下列说法中能表示达到平衡状态的是bc(填序号).
a.四种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比
b.单位时间内断开amol H-H键的同时断开2a mol O-H键
c.反应容器中放出的热量不再变化
d.混合气体的密度不再发生变化
e.混合气体的压强不再发生变化
(4)某温度下,第Ⅱ步反应的平衡常数为K=$\frac{1}{9}$.该温度下在甲、乙、丙三个恒容密闭容器中投入H2O(g)和CO(g),其起始浓度如下表所示.下列判断不正确的是CD.
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2O)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO)/mol/L | 0.010 | 0.010 | 0.020 |
B.平衡时,甲中和丙中H2O的转化率均是25%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.015mol/L
D.平衡时,乙中H2O的转化率大于25%
 已知2SO2(g)十O2(g)$?_{催化剂}^{加热}$ 2SO3(g)反应过程的能量变化如图所示.请回答下列问题:
已知2SO2(g)十O2(g)$?_{催化剂}^{加热}$ 2SO3(g)反应过程的能量变化如图所示.请回答下列问题: 2,4,4-三甲基己烷,
2,4,4-三甲基己烷, .
.