题目内容
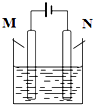 如图所示,用石墨作电极电解氯化铜溶液,下列说法正确的是( )
如图所示,用石墨作电极电解氯化铜溶液,下列说法正确的是( )分析:用石墨作电极电解氯化铜溶液,连接电源正极的为电解池的阳极,发生氧化反应:2Cl--2e-=Cl2↑,连接电源负极的为电解池的阴极,发生:Cu2++2e-=Cu,电解池工作时,阴离子向阳极移动,阳离子向阴极移动,以此解答该题.
解答:解:A.M极连接电源的正极,为电解池的阳极,故A错误;
B.阴离子向阳极移动,即向M极移动,故B错误;
C.M极上发生氧化反应:2Cl--2e-=Cl2↑,生成的氯气具有氧化性,可氧化碘化钾生成碘单质,试纸变蓝,故C正确;
D.在M、N两极流过0.4mol e-时,N极发生:Cu2++2e-=Cu,析出0.2mol铜,即12.8g,故D错误.
故选C.
B.阴离子向阳极移动,即向M极移动,故B错误;
C.M极上发生氧化反应:2Cl--2e-=Cl2↑,生成的氯气具有氧化性,可氧化碘化钾生成碘单质,试纸变蓝,故C正确;
D.在M、N两极流过0.4mol e-时,N极发生:Cu2++2e-=Cu,析出0.2mol铜,即12.8g,故D错误.
故选C.
点评:本题考查电解池知识,题目难度不大,注意把握电极的判断以及电极方程式的书写,为解答该题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


 (2013?通州区二模)碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式.
(2013?通州区二模)碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式.