题目内容
10.对食物的酸、碱性判断正确的是( )| A. | 苹果是酸性食物 | B. | 梨、桃是碱性食物 | ||
| C. | 猪肉、牛肉是碱性食物 | D. | 巧克力、奶油是碱性食物 |
分析 酸性食物:含硫、磷、氯等矿物质较多的食物,在体内的最终代谢产物常呈酸性,如肉、蛋鱼等动物食品及豆类和谷类等.
碱性食物:含钾、钠、钙、镁等矿物质较多的食物,在体内的最终的代谢产物常呈碱性,如,蔬菜、水果、乳类、大豆和菌类等.
解答 解:A.苹果属于水果,在体内的最终的代谢产物常呈碱性,属于碱性食物,故A错误;
B.梨、桃属于水果,在体内的最终的代谢产物常呈碱性,属于碱性食物,故B正确;
C.猪肉、牛肉富含蛋白质,在体内的最终代谢产物常含氮,属于酸性食物,故C错误;
D.巧克力、奶油富含脂肪,在体内的最终代谢产物常呈酸性,属于酸性食物,故D错误.
故选B.
点评 本题考查了食物的酸碱性,难度不大,判断食物的酸碱性,并非根据人们的味觉、也不是根据食物溶于水中的化学性,而是根据食物进入人体后所生成的最终代谢物的酸碱性而定.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.x、y、z为三种气体,把a mol x和b mol y充入一密闭容器中,发生反应,x+2y?2z达到平衡时,若它们的物质的量满足n(x)+n(y)=n(z),则y的转化率为( )
| A. | $\frac{a+b}{5×100%}$ | B. | $\frac{2(a+b)}{5b×100%}$ | C. | $\frac{200(a+b)}{5b}$% | D. | $\frac{(a+b)}{5a×100%}$ |
18.化学与生产、生活密切相关,下列说不正确的是( )
| A. | 合成纤维和光导纤维都属于新型无机非金属材料 | |
| B. | “地沟油”禁止食用,但经过加T处理后,可以用来制取肥皂和生物柴油 | |
| C. | 大力推广应用“脱硫、脱硝”技术,可减少硫氧化物、氮氧化物对空气的污染 | |
| D. | 利用丁达尔效应鉴别 Fe(OH)3胶体和FeCl3溶液 |
5.下列现象与胶体的性质无关的是( )
| A. | 早晨的树林里会看到太阳透过树叶射出的美丽光束 | |
| B. | 浑浊的水可以用明矾净化 | |
| C. | 向FeCl3溶液中加入NaOH溶液,会出现红褐色沉淀 | |
| D. | 尿毒症患者做“血液透析” |
2.下列说法不正确的是( )
| A. | 加入苯酚显紫色的溶液:K+、NH4+、Cl-、I-;加入酚酞呈红色的溶液:SO42-、K+、Cl-、HSO3-分别都不能大量共存(常温下) | |
| B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:K+、AlO2-、CO32-、Na+; pH=2的溶液:NO3-、Fe2+、Na+、Al3+分别都可以大量共存(常温下) | |
| C. | 已知:25℃时,Mg(OH)2的Ksp=5.61×10-12,MgF2的KSP=7.42×10-11,25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2 可以转化为MgF2 | |
| D. | 表示H2燃烧热的化学方程式为:H2(g)+$\frac{1}{2}$O2(g)═H2O(1);△H=-285.8kJ/mol |
17.乙酸正丁酯是无色透明有愉快果香气味的液体,可由乙酸和正丁醇制备.反应的化学方程式如下:
CH3COOH+CH2CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O
发生的副反应如下:2CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$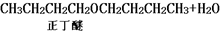
CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$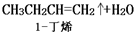
有关化合物的物理性质见表:
已知:乙酸正丁酯、正丁醇和水组成三元共沸物恒沸点为90.7℃.
合成:
方案甲:采用装置甲(分水器预先加入水,使水面略低于分水器的支管口),在干燥的50mL圆底烧瓶中,加入13.8mL(0.150mol)正丁醇和7.2mL(0.125mol)冰醋酸,再加入3~4滴浓硫酸和2g沸石,摇匀.按下图安装好带分水器的回流反应装置,通冷却水,圆底烧瓶在电热套上加热煮沸.在反应过程中,通过分水器下部的旋塞分出生成的水(注意保持分水器中水层液面仍保持原来高度,使油层尽量回到圆底烧瓶中).反应基本完成后,停止加热.
方案乙:采用装置乙,加料方式与方案甲相同.加热回流,反应60min后停止加热.
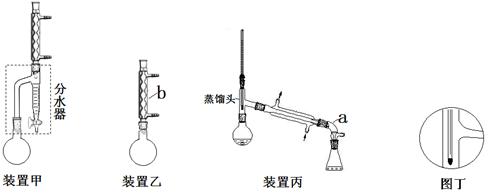
提纯:甲乙两方案均采用蒸馏方法.操作如下:

请回答:
(1)方案甲中使用分水器不断分离除去水的目的是有利于平衡向生成乙酸正丁酯的反应方向移动.
(2)仪器a的名称接受器或牛角管,仪器b的名称球形冷凝管.
(3)提纯过程中,步骤②的目的是为了除去有机层中残留的酸,步骤④加入少量无水MgSO4的目的是干燥.
(4)下列有关洗涤过程中分液漏斗的使用正确的是AB.
A.分液漏斗使用前必须要检漏,只要分液漏斗的玻璃塞和旋塞芯处不漏水即可使用
B.洗涤时振摇放气操作应如图所示

C.放出下层液体时,不需将要玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
D.洗涤完成后,先放出下层液体,然后继续从下口放出有机层置于干燥的锥形瓶中
(5)按装置丙蒸馏,最后圆底烧瓶中残留的液体主要是正丁醚;若按图丁放置温度计,则收集到的产品馏分中还含有正丁醇.
(6)实验结果表明方案甲的产率较高,原因是通过分水器及时分离出产物水,有利于酯化反应的进行,提高酯的产率.
CH3COOH+CH2CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O
发生的副反应如下:2CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$
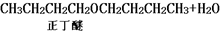
CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$
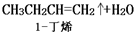
有关化合物的物理性质见表:
| 化合物 | 密度(g•cm-3) | 水溶性 | 沸点(℃) |
| 冰乙酸 | 1.05 | 易溶 | 118.1 |
| 正丁醇 | 0.80 | 微溶 | 117.2 |
| 正丁醚 | 0.77 | 不溶 | 142.0 |
| 乙酸正丁酯 | 0.90 | 微溶 | 126.5 |
合成:
方案甲:采用装置甲(分水器预先加入水,使水面略低于分水器的支管口),在干燥的50mL圆底烧瓶中,加入13.8mL(0.150mol)正丁醇和7.2mL(0.125mol)冰醋酸,再加入3~4滴浓硫酸和2g沸石,摇匀.按下图安装好带分水器的回流反应装置,通冷却水,圆底烧瓶在电热套上加热煮沸.在反应过程中,通过分水器下部的旋塞分出生成的水(注意保持分水器中水层液面仍保持原来高度,使油层尽量回到圆底烧瓶中).反应基本完成后,停止加热.
方案乙:采用装置乙,加料方式与方案甲相同.加热回流,反应60min后停止加热.

提纯:甲乙两方案均采用蒸馏方法.操作如下:

请回答:
(1)方案甲中使用分水器不断分离除去水的目的是有利于平衡向生成乙酸正丁酯的反应方向移动.
(2)仪器a的名称接受器或牛角管,仪器b的名称球形冷凝管.
(3)提纯过程中,步骤②的目的是为了除去有机层中残留的酸,步骤④加入少量无水MgSO4的目的是干燥.
(4)下列有关洗涤过程中分液漏斗的使用正确的是AB.
A.分液漏斗使用前必须要检漏,只要分液漏斗的玻璃塞和旋塞芯处不漏水即可使用
B.洗涤时振摇放气操作应如图所示

C.放出下层液体时,不需将要玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
D.洗涤完成后,先放出下层液体,然后继续从下口放出有机层置于干燥的锥形瓶中
(5)按装置丙蒸馏,最后圆底烧瓶中残留的液体主要是正丁醚;若按图丁放置温度计,则收集到的产品馏分中还含有正丁醇.
(6)实验结果表明方案甲的产率较高,原因是通过分水器及时分离出产物水,有利于酯化反应的进行,提高酯的产率.
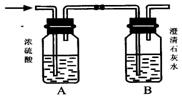 某混合气体X含H2、CO、CH4中的一种或几种组成.将X气体燃烧,把燃烧后生成的气体通过A、B两个洗气瓶.试回答下列问题:
某混合气体X含H2、CO、CH4中的一种或几种组成.将X气体燃烧,把燃烧后生成的气体通过A、B两个洗气瓶.试回答下列问题: