题目内容
pH=3的CH3COOH、H2SO4、HNO3、HCl溶液中,分别加入足量的Zn粉,当三种溶液的体积相同时,下列说法正确的是( )
| A、CH3COOH放出的H2最多 |
| B、HNO3中放出的H2最多 |
| C、H2SO4放出的H2最多 |
| D、HCl,HNO3放出的H2最多 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:H2SO4、HCl、HNO3为强酸,CH3COOH为弱酸,等pH时,CH3COOH浓度最大,H2SO4浓度最小,由于HNO3具有强氧化性,与锌粉反应不生成氢气,以此解答该题.
解答:
解:CH3COOH为弱酸,等pH时,CH3COOH浓度最大,则醋酸放出的氢气最多,故C错误、A正确;由于HNO3具有强氧化性,与锌粉反应不生成氢气,故B、D错误.
故选A.
故选A.
点评:本题考查较为综合弱电解质的电离和硝酸的性质,综合考查学生的分析能力和元素化合物知识的应用能力,为高考常见题型,难度中等,注意硝酸具有强氧化性的性质,为该题的易错点.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
下列叙述不正确的是( )
| A、苯与氢气反应属于加成反应 |
| B、苯与硝酸的反应是加成反应 |
| C、苯与液溴生成溴苯 |
| D、苯能够萃取溴水中的溴 |
下列有机物检验方法正确的是( )
| A、取少量卤代烃加入NaOH水溶液共热,冷却,再加入AgNO3溶液检验卤代烃中卤原子的存在 |
| B、淀粉用酸催化水解后的溶液加入新制银氨溶液,水浴加热,来检验葡萄糖 |
| C、通过红外光谱分析可以区分乙醇和乙酸乙酯 |
| D、用新制CaO检验乙醇中是否含有水分 |
下列物质中,含有离子键的化合物是( )
| A、KOH |
| B、H2O |
| C、HCl |
| D、H2 |
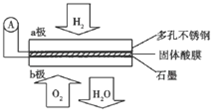 某固体酸燃料电池以Ca(HSO4)2固体为电解质传递H+,其基本结构如图,电池总反应可表示为:2H2+O2═2H2O,下列有关说法正确的是( )
某固体酸燃料电池以Ca(HSO4)2固体为电解质传递H+,其基本结构如图,电池总反应可表示为:2H2+O2═2H2O,下列有关说法正确的是( )| A、电子通过外电路从b极流向a极 |
| B、b极上的电极反应式为:O2+2H2O+4e-═4OH- |
| C、每转移0.1mol电子,消耗1.12L的H2 |
| D、H+由a极通过固体酸电解质传递到b极 |
把11克金属混合物加入足量的稀H2SO4中,在标准状况下产生0.5mol气体,则混合物中所含的金属可能是( )
| A、Al和Mg |
| B、Al和Zn |
| C、Zn和Fe |
| D、Fe和Mg |
对相同质量的N2与NO作比较,正确的是( )
| A、所含的分子数相等 |
| B、在同温同压下,V(N2)═V(NO) |
| C、所含的原子数不相等 |
| D、在同温同体积下,p(N2)<p(NO) |
化学与工农业生产和人类生活密切相关.下列说法中错误的是( )
| A、晶体硅是良好的半导体材料,是信息技术的关键材料 |
| B、华裔科学家高琨在光纤传输信息领域中取得突破性成就,光纤的主要成分是高纯度的单质硅 |
| C、硅胶常用于作干燥剂 |
| D、硅酸钠的水溶液俗称水玻璃,可用于制备木材防火剂 |