题目内容
10.下列化合物不能由化合反应得到的是( )| A. | FeS | B. | CuS | C. | SO3 | D. | FeCl3 |
分析 氯气具有强氧化性,与变价金属生成高价金属氯化物;S具有弱氧化性,与变价金属生成低价金属硫化物,二氧化硫与氧气反应生成三氧化硫,以此来解答.
解答 解:A.Fe与S加热发生化合反应生成FeS,故A不选;
B.Cu与S加热发生化合反应生成Cu2S,故B选;
C.二氧化硫与氧气发生催化氧化反应生成三氧化硫,为化合反应,故C不选;
D.Fe与氯气加热发生化合反应生成FeCl3,故D不选;
故选B.
点评 本题考查金属的性质,为高频考点,把握物质的性质、发生的氧化还原反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
20.下列分散系中,能产生“丁达尔效应”的是( )
| A. | Na2SO4溶液 | B. | NH4Cl溶液 | C. | 石灰乳 | D. | Fe(OH)3胶体 |
18.X、Y、Z、W四种气体都是污染大气的物质,其中Y跟W按一定体积比相遇时可消除气体的毒性;Y跟Z相遇时,可使气体的红棕色变浅;Y与Z分别是引起酸雨的主要物质,这四种气体依次是( )
| A. | H2S、NO、HCl、SO2 | B. | SO2、HCl、NO2、H2S | C. | H2S、NO2、Cl2、SO2 | D. | Cl2、SO2、NO2、H2S |
5.在30mL18mol/LH2SO4溶液中加入12g碳,加热,充分反应后被还原的H2SO4的物质的量为( )
| A. | 等于0.54mol | B. | 小于0.54mol | C. | 等于1.00mol | D. | 大于1.00mol |
15.质量分数为25%的氨水的密度是0.92g/cm3,质量分数为5%的氨水的密度是0.98g/cm3,将这两种氨水等体积混合,混合后所得氨水的质量分数( )
| A. | 等于15% | B. | 大于15% | C. | 小于15% | D. | 无法判断 |
2.关于Na2CO3和NaHCO3性质的有关叙述正确的是( )
| A. | 在水中的溶解性:Na2CO3<NaHCO3 | B. | 热稳定性:Na2CO3<NaHCO3 | ||
| C. | NaHCO3能转化为Na2CO3 | D. | Na2CO3不能转化成NaHCO3 |
3.下列离子方程式正确的是( )
| A. | 澄清的石灰水与盐酸反应 Ca(OH)2+2H+═Ca2++2H2 O | |
| B. | 钠与水的反应 Na+2H2 O═Na++2OH-+H2↑ | |
| C. | 铜片插入硝酸银溶液 Cu+Ag+═Cu2++Ag | |
| D. | 大理石溶于醋酸 CaCO3+2 CH3COOH═Ca2++2 CH3COO-+H2O+CO2↑ |
4.下列实验操作或装置能达到实验目的是( )
| A. |  量取109.3mL稀盐酸 | B. |  称量25g烧碱固体 | ||
| C. |  碳酸氢钠受热分解 | D. | 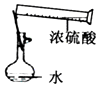 配制一定物质的量浓度的稀硫酸 |