题目内容
下列叙述正确的是( )
| A、将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2,产生沉淀 |
| B、在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解 |
| C、向AlCl3溶液中滴加氨水,产生白色沉淀;再加入NaHSO4溶液,沉淀消失 |
| D、除去FeCl2中少量的FeBr2,加入适量氯水;再加四氯化碳萃取分液 |
考点:二氧化硫的化学性质,镁、铝的重要化合物,铁盐和亚铁盐的相互转变,铜金属及其重要化合物的主要性质
专题:元素及其化合物
分析:A.HCl酸性大于碳酸、亚硫酸,CO2、SO2和BaCl2溶液不反应;
B.酸性条件下,硝酸根离子具有强氧化性,能氧化Cu;
C.氢氧化铝能溶于强酸、强碱溶液;
D.氯气具有强氧化性,能将亚铁离子氧化铁离子,将溴离子氧化为溴单质,且先氧化亚铁离子.
B.酸性条件下,硝酸根离子具有强氧化性,能氧化Cu;
C.氢氧化铝能溶于强酸、强碱溶液;
D.氯气具有强氧化性,能将亚铁离子氧化铁离子,将溴离子氧化为溴单质,且先氧化亚铁离子.
解答:
解:A.HCl酸性大于碳酸、亚硫酸,CO2、SO2和BaCl2溶液不反应,则没有沉淀生成,故A错误;
B.酸性条件下,硝酸根离子具有强氧化性,能氧化Cu,在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO3)2固体,溶液中相当于有硝酸,硝酸和铜发生氧化还原反应而铜粉溶解,故B错误;
C.氢氧化铝能溶于强酸、强碱溶液,AlCl3溶液中滴加氨水,生成氢氧化铝白色沉淀,NaHSO4能电离出氢离子而使溶液呈强酸性,能溶液氢氧化铝,所以沉淀溶解,故C正确;
D.氯气具有强氧化性,能将亚铁离子氧化铁离子,将溴离子氧化为溴单质,且先氧化亚铁离子,所以加入氯水先将亚铁离子氧化后氧化溴离子,所以得不到氯化亚铁,故D错误;
故选C.
B.酸性条件下,硝酸根离子具有强氧化性,能氧化Cu,在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO3)2固体,溶液中相当于有硝酸,硝酸和铜发生氧化还原反应而铜粉溶解,故B错误;
C.氢氧化铝能溶于强酸、强碱溶液,AlCl3溶液中滴加氨水,生成氢氧化铝白色沉淀,NaHSO4能电离出氢离子而使溶液呈强酸性,能溶液氢氧化铝,所以沉淀溶解,故C正确;
D.氯气具有强氧化性,能将亚铁离子氧化铁离子,将溴离子氧化为溴单质,且先氧化亚铁离子,所以加入氯水先将亚铁离子氧化后氧化溴离子,所以得不到氯化亚铁,故D错误;
故选C.
点评:本题考查物质之间的反应,涉及复分解反应、氧化还原反应、离子反应,侧重考查基本理论,明确物质的性质是解本题关键,易错选项是B,注意隐含条件.

练习册系列答案
相关题目
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )
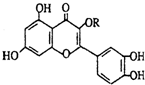

| A、可以和溴水反应 |
| B、可溶于有机溶剂 |
| C、该有机物分子难以被氧化 |
| D、1mol维生素P最多可以和4molNaOH反应 |
下列说法正确的是( )
| A、化学家采用玛瑙研钵摩擦固体进行无溶剂合成,玛瑙的主要成分是硅酸盐 |
| B、蛋白质溶液遇硫酸铜后产生的沉淀,加水又能重新溶解 |
| C、石油经分馏可得到汽油、煤油、柴油、煤焦油等含碳原子数比较少的轻质油 |
| D、工业规模海水中提溴的常用方法是空气吹出法 |
下列物质的电子式,正确的是( )
A、 |
B、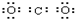 |
C、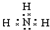 |
D、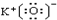 |
将羧酸的碱金属盐电解可生成烃类化合物,例如:2CH3COOK+2H2O
CH3-CH3↑+2CO2↑+H2↑+2KOH
现充分电解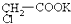 水溶液,并加热电解后的水溶液,则下列说法中合理的是( )
水溶液,并加热电解后的水溶液,则下列说法中合理的是( )
| ||
现充分电解
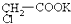 水溶液,并加热电解后的水溶液,则下列说法中合理的是( )
水溶液,并加热电解后的水溶液,则下列说法中合理的是( )| A、CO2气体在阴极放出 |
| B、加热后有不溶于水的油状物生成 |
| C、混合液蒸干后得到的固体物质是KOH |
| D、混合液蒸干后得到的固体物质是KCl |
化学与生产、生活密切相关,下列有关叙述正确的是( )
| A、晶体硅是“信息革命“的支柱材料,可用作光导纤维 |
| B、将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
| C、化学反应伴随着能量的变化,反应物总能量一定大于生成物总能量 |
| D、用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的 |
能够可把苯酚水溶液、乙醇、氢氧化钠溶液鉴别出来的试剂是( )
| A、水 | B、酸性高锰酸钾溶液 |
| C、己烷 | D、饱和溴水 |