题目内容
实验探究:探究碳、硅元素的非金属性的相对强弱
根据要求完成下列各小题
(1)实验装置:
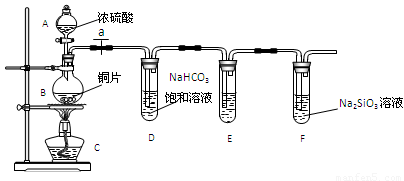
填写所示仪器名称A B
(2)实验步骤:
连接仪器、_____________、加药品后,打开a、然后滴入浓硫酸,加热
(3)问题探究:(已知酸性强弱:亚硫酸 >碳酸)
①铜与浓硫酸反应的化学方程式是 ;
装置E中足量酸性KMnO4溶液的作用是 ;
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是 ;
③依据试管D中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性___(填“能”或“否”),试管D中发生反应的离子方程式是
(10分)(1)A:分液漏斗B:圆底烧瓶(每空1分)(2)检查装置的气密性(1分)
(3)①Cu+2H2SO4(浓)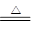 CuSO4+ SO2↑+2H2O
(2分) 除去SO2气体(1分)
CuSO4+ SO2↑+2H2O
(2分) 除去SO2气体(1分)
②盛有Na2SiO3溶液的试管中出现白色沉淀(1分) ③否(1分)
SO2+2HCO3-=SO32-+ H2O+CO2↑或SO2+HCO3-=HSO3-+CO2↑(2分)
【解析】
试题分析:(1)根据仪器的结构特点可知,A是分液漏斗,B是圆底烧瓶。
(2)连接仪器之后,必须检查装置的气密性。
(3)①浓硫酸具有强氧化性,在加热的条件下,铜与浓硫酸反应的化学方程式是Cu+2H2SO4(浓)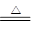 CuSO4+ SO2↑+2H2O。由于从装置D中出来的气体可能含有SO2,会干扰实验,所以酸性高锰酸钾溶液的作用是除去SO2气体。
CuSO4+ SO2↑+2H2O。由于从装置D中出来的气体可能含有SO2,会干扰实验,所以酸性高锰酸钾溶液的作用是除去SO2气体。
②根据较强的酸制备较弱的酸可知,盛有Na2SiO3溶液的试管中出现白色沉淀时,即可以说明碳元素的非金属性比硅元素非金属性强。
③S元素的最高价氧化物的水化物是硫酸,而与D中碳酸氢钠反应的是亚硫酸,所以不能依据试管D中的实验现象,来证明硫元素的非金属性强于碳元素的非金属性。D中发生反应的离子方程式是SO2+2HCO3-=SO32-+ H2O+CO2↑或SO2+HCO3-=HSO3-+CO2↑。
考点:考查碳、硅元素的非金属性的相对强弱的实验探究
点评:该题是中等难度的试题,试题综合性强,侧重对学生实验探究能力的培养,有利于激发学生的学习积极性,也有助于培养学生的规范实验设计能力。该题的关键是1.准确地把握实验目的;2.利用已学知识,分析如何实现这个目的——实验原理;3.结合实验材料,初步确定设计对策--实验方案。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案


