题目内容
8.煤矸石是采煤和洗煤时的废弃物,其主要成分是Al2O3、SiO2,另外还含有数量不等的Fe2O3、CaO、MgO、Na2O、K2O、P2O5、SO3等.下列关于煤矸石的说法正确的是( )| A. | 煤矸石中的金属氧化物均溶于水,且都能与水反应 | |
| B. | 煤矸石含有的酸性氧化物对应的水化物中,酸性最强的是H3PO4 | |
| C. | 煤矸石可用于生产矸石水泥、耐火砖等建筑材料 | |
| D. | 用盐酸可以溶解煤矸石中的所有氧化物 |
分析 A、Al2O3、SiO2均难溶于水;
B、P2O5和SO3对应水化物的酸为磷酸、硫酸,硫酸酸性强;
C、煤矸石主要成分是Al2O3、SiO2,熔点高硬度大;
D、SiO2不能溶于盐酸.
解答 解:A、煤矸石主要成分是Al2O3、SiO2,Al2O3、SiO2均难溶于水,故A错误;
B、P2O5和SO3对应水化物的酸为磷酸、硫酸,硫酸为强酸,所以酸性较强的是H2SO4,故B错误;
C、煤矸石主要成分是Al2O3、SiO2,可用于生产矸石水泥、耐火砖等建筑材料,故C正确;
D、SiO2不能溶于盐酸,所以用盐酸可以溶解煤矸石中的部分氧化物如Al2O3,而SiO2不能溶,故D错误.
故选:C.
点评 本题考查了物质分类方法和物质性质的判断,主要是两性氧化物、碱性氧化物性质的分析判断,掌握基础是关键,题目较简单.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
19.除去括号内杂质的试剂或方法错误的是( )
| A. | KNO3晶体(NaCl),蒸馏水,结晶 | |
| B. | CO2(SO2),酸性KMnO4溶液、浓硫酸,洗气 | |
| C. | HNO3溶液(H2SO4),适量BaCl2溶液,过滤 | |
| D. | C2H5OH(CH3COOH),加足量CaO,蒸馏 |
16.A、B、C、D、E、F六种化合物,其中A、B、C、D、E均由短周期元素组成,焰色反应均为黄色,B、C、E均由三种元素组成.B、C的组成元素相同,且C的摩尔质量比B大80g/mol,回答:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为AC
A、离子键 B、极性共价键 C、非极性共价键 D、氢键
(2)下表为B与F实验的部分内容
写出B与稀H2SO4反应的离子方程式S2O32-+2H+=S↓+SO2↑+H2O,
写出②中反应方程式FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl;
(3)现由6种粒子Mn2+、MnO4-、H+、H2O、X2Y82-(C中含有的阴离子)、XY42-完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO4-需氧化剂的物质的量为2.5mol
(4)化合物D和E相互转化D$?_{CO_{2}+H_{2}O}^{△}$ E,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为AC
A、离子键 B、极性共价键 C、非极性共价键 D、氢键
(2)下表为B与F实验的部分内容
| ①在含B的溶液中加入稀H2SO4,产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 |
| ②20mL沸水中滴加F的饱和溶液1~2mL所得液体呈红褐色 |
| ③将实验②得到的红褐色液体加热蒸发,灼烧,最终得到红棕色固体 |
写出②中反应方程式FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl;
(3)现由6种粒子Mn2+、MnO4-、H+、H2O、X2Y82-(C中含有的阴离子)、XY42-完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO4-需氧化剂的物质的量为2.5mol
(4)化合物D和E相互转化D$?_{CO_{2}+H_{2}O}^{△}$ E,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.
13.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 1mol N2所含有的原子数为NA | |
| B. | 1mol•L-1 NaCl溶液中含有的钠离子数目为NA | |
| C. | 标准状况下,22.4 LCO所含的原子数为NA | |
| D. | 12.4g白磷(分子式为P4)中含有磷原子数为0.4NA |
20.下列反应中,电子转移发生在同种元素之间的是( )
| A. | Fe+Cu2+=Fe2++Cu | B. | 2H2S+SO2=3S+2H2O | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | D. | 2H2O $\frac{\underline{\;电解\;}}{\;}$ 2H2↑+O2↑ |
17.用水稀释0.1mol/L一元弱酸HX时,溶液中随着水量的增加而增大的是( )
| A. | c(H+) | B. | c(X-) | C. | $\frac{c({H}^{+})}{c(HX)}$ | D. | $\frac{c(HX)}{c({H}^{+})}$ |
18.在298K1.0l×l05Pa下,将32gSO2通入750mL 1mol/L KOH溶液中充分反应.测得反应放出xkJ的热量.已知在该条件下,lmolSO2通入1L 2mol/L KOH溶液中充分反应放出ykJ的热量.则SO2与KOH溶液反应生成KHSO3的热化学方程式正确的是( )
| A. | SO2(g)+KOH(aq)═KHSO3(aq)△H=-(4x-y)kJ/mol | |
| B. | SO2(g)+KOH(aq)═KHSO3(aq)△H=-(2x-y)kJ/mol | |
| C. | SO2(g)+KOH(aq)═KHSO3(aq)△H=-(2y-x)kJ/mol | |
| D. | 2SO2(g)+2KOH(1)═2KHSO3(1)△H=-(8x-2y)kJ/mol |
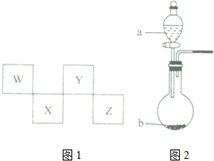 W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.
W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.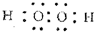 ,Z在周期表中的位置第三周期ⅦA族.
,Z在周期表中的位置第三周期ⅦA族. 以氨作为燃料的固体氧化物(含有02-)燃料电池,具有全固态结构、能量效率高、无污染等特点,另外氨气含氢量高,不含碳,易液化,方便运输和贮存,是很好的氢源载体.其工作原理如图所示:
以氨作为燃料的固体氧化物(含有02-)燃料电池,具有全固态结构、能量效率高、无污染等特点,另外氨气含氢量高,不含碳,易液化,方便运输和贮存,是很好的氢源载体.其工作原理如图所示: