题目内容
13.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )| A. | 1mol N2所含有的原子数为NA | |
| B. | 1mol•L-1 NaCl溶液中含有的钠离子数目为NA | |
| C. | 标准状况下,22.4 LCO所含的原子数为NA | |
| D. | 12.4g白磷(分子式为P4)中含有磷原子数为0.4NA |
分析 A、氮气为双原子分子;
B、溶液体积不明确;
C、求出CO的物质的量,然后根据CO为双原子分子来分析;
D、白磷由磷原子构成.
解答 解:A、氮气为双原子分子,故1mol氮气中含2mol氮原子即2NA个,故A错误;
B、溶液体积不明确,故溶液中的钠离子的个数无法计算,故B错误;
C、标况下22.4LCO的物质的量为1mol,而CO为双原子分子,故1molCO中含2mol原子即2NA个,故C错误;
D、白磷由磷原子构成,故12.4g白磷中含有的磷原子的物质的量n=$\frac{12.4g}{31g/mol}$=0.4mol,个数为0.4NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
3.由不同种类的原子组成的物质可能是( )
①纯净物
②混合物
③单质
④化合物
⑤金属
⑥非金属
⑦酸
⑧碱
⑨盐
⑩氧化物.
①纯净物
②混合物
③单质
④化合物
⑤金属
⑥非金属
⑦酸
⑧碱
⑨盐
⑩氧化物.
| A. | ①③⑤⑦⑨ | B. | ②④⑧⑩ | C. | ①③ | D. | 全部 |
4.在2L密闭容器内,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
(1)用O2表示从0~2s内该反应的平均速率v=0.015mol•L-1•S-1.
(2)能说明该反应已经达到平衡状态的是AD
A.容器内压强不变 B.容器内气体的密度保持不变
C.v正(NO)=2v正(O2) D.v正(NO2)=v逆(NO2)
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
(2)能说明该反应已经达到平衡状态的是AD
A.容器内压强不变 B.容器内气体的密度保持不变
C.v正(NO)=2v正(O2) D.v正(NO2)=v逆(NO2)
8.煤矸石是采煤和洗煤时的废弃物,其主要成分是Al2O3、SiO2,另外还含有数量不等的Fe2O3、CaO、MgO、Na2O、K2O、P2O5、SO3等.下列关于煤矸石的说法正确的是( )
| A. | 煤矸石中的金属氧化物均溶于水,且都能与水反应 | |
| B. | 煤矸石含有的酸性氧化物对应的水化物中,酸性最强的是H3PO4 | |
| C. | 煤矸石可用于生产矸石水泥、耐火砖等建筑材料 | |
| D. | 用盐酸可以溶解煤矸石中的所有氧化物 |
5.下列有关说法不正确的是( )
| A. | 镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 | |
| B. | 手机上用的锂离子电池属于二次电池 | |
| C. | 燃料电池能把化学能转化成电能 | |
| D. | 已知反应2CO(g)=2C(s)+O2(g)的△H>0、△S<0,那么高温下可自发进行 |
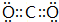 .
. .
. 五氧化二碘可用于消除CO的污染,也可定量测定CO含量,其反应原理为
五氧化二碘可用于消除CO的污染,也可定量测定CO含量,其反应原理为