题目内容
下列化学用语表达正确的是( )
A、对-硝基甲苯的结构简式: |
B、CH2F2的电子式: |
| C、16O2与18O2互为同素异形体 |
| D、乙炔的最简式:CH |
考点:电子式、化学式或化学符号及名称的综合,同素异形体,结构简式
专题:
分析:A.硝基的表示方法错误,写在苯环左边时应该表示为:O2N-;
B.该电子式中没有表示出氟原子的3对未成键电子;
C.同素异形体为同种元素形成的不同种单质,16O2与18O2为同一种物质;
D.乙炔分子中含有2个C、2个H原则,其最简式为CH.
B.该电子式中没有表示出氟原子的3对未成键电子;
C.同素异形体为同种元素形成的不同种单质,16O2与18O2为同一种物质;
D.乙炔分子中含有2个C、2个H原则,其最简式为CH.
解答:
解:A.对-硝基甲苯的结构简式中,硝基应该表示为O2N-,其正确的结构简式为: ,故A错误;
,故A错误;
B.CH2F2的电子式中,氟原子最外层达到8电子稳定结构,其正确的电子式为: ,故B错误;
,故B错误;
C.16O2与18O2都是氧气单质,为同一种物质,不属于同素异形体,故C错误;
D.最简式为分子中各原子的最简比,乙炔分子中含有2个C、2个H,则其最简式为CH,故D正确;
故选D.
 ,故A错误;
,故A错误;B.CH2F2的电子式中,氟原子最外层达到8电子稳定结构,其正确的电子式为:
 ,故B错误;
,故B错误;C.16O2与18O2都是氧气单质,为同一种物质,不属于同素异形体,故C错误;
D.最简式为分子中各原子的最简比,乙炔分子中含有2个C、2个H,则其最简式为CH,故D正确;
故选D.
点评:本题考查了最简式、电子式、结构简式、同素异形体的判断,题目难度中等,注意掌握常见化学用语的书写方法,明确最简式与结构简式、结构简式的区别,选项A为易错点,注意硝基的表示方法.

练习册系列答案
相关题目
下列物质不能通过单质间化合反应直接生成的物质是( )
| A、FeCl2 |
| B、CuCl2 |
| C、NaCl |
| D、AlCl3 |
下列有关说法正确的是( )
| A、活化分子的总数越多,反应速率越快 |
| B、升高温度,活化分子百分数不变,活化分子数增多,化学反应速率增大 |
| C、使用催化剂,降低了反应的活化能,增大了活化分子百分数,化学反应速率增大 |
| D、加入反应物,使活化分子百分数增大,化学反应速率增大 |
将0.2mol钠、镁、铝分别放入100mL1mol?L-1的盐酸中,产生的气体体积比是(气体体积在同温同压下测得)( )
| A、1:2:3 |
| B、6:3:2 |
| C、1:1:1 |
| D、2:1:1 |
有关化学用语的表示正确的是( )
| A、HCN分子的结构式:H-C≡N |
B、二氧化碳的电子式: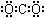 |
C、Cl-的结构示意图为: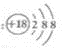 |
| D、乙烯的结构简式为CH2CH2 |
下列叙述正确的是( )
| A、1.00 mol NaCl中含有6.02×1023个NaCl分子 |
| B、1.00 mol NaCl中,所有Na+的最外层电子总数为10×6.02×1023 |
| C、欲配置1.00L、1.00 mol.L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 |
| D、1mol Fe与稀硫酸反应Fe失去的电子数为2NA |
下列电离方程式的书写正确的是( )
| A、CuCl2=Cu+Cl2↑ |
| B、H2SO4=2H++S6++4O2- |
| C、Na2CO3=2Na++CO32- |
| D、Ba(OH)2=Ba+2OH |
