题目内容
13.除去NaCl中少量杂质CaCl2 Na2SO4,所用试剂及顺序正确的是( )| A. | Na2CO3、BaCl2、HCl | B. | BaCl2、Na2CO3、HCl | ||
| C. | BaCl2、Na2CO3、HNO3 | D. | BaCl2、K2CO3、HNO3 |
分析 利用氯化钡除去硫酸根离子,利用碳酸钠除去钙离子,且碳酸钠在氯化钡之后可除去过量的钡离子,最后加盐酸,以此来解答.
解答 解:除去NaCl中少量杂质CaCl2 Na2SO4,先加足量BaCl2,除去硫酸根离子,然后加足量Na2CO3,除去钙离子,且碳酸钠在氯化钡之后可除去过量的钡离子,最后加适量盐酸,除去碳酸根离子,
不能选K2CO3、HNO3,引入新杂质不能除去,
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应及试剂的加入顺序为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
4.不考虑水的电离,下列水溶液中的四种离子可以大量共存,且物质的量浓度也相等的是( )
| A. | Na+、K+、MnO4-、NO3- | B. | ClO-、I-、NH4+、Ba2+ | ||
| C. | Na+、AlO2-、K+、HCO3- | D. | Al3+、K+、SO42-、NO3- |
1.设NA为阿伏加德罗常数的值.则下列说法不正确的是( )
| A. | 4.6g 金属钠与足量O2充分反应后,所得固体中阴、阳离子的总数为0.3NA | |
| B. | 1 L 0.5 mol/L 的FeCl3溶液充分水解后,所得Fe(OH)3胶粒的数目为0.5NA | |
| C. | 过量的Fe与1 mol Cl2充分反应,转移电子的数目为2NA | |
| D. | 1 L含NA个Al3+的Al(NO3)3溶液中,NO3-物质的量浓度大于3 mol/L |
18.某含铬(Cr2O72-)废水用硫酸亚铁铵废水用硫酸亚铁铵[FeSO4•(NH4)2SO4•6H2O]处理,反应中铁元素和铬元素完全转化为沉淀.该沉淀经干燥后得到n molFeO•FeyCrxO3.不考虑处理过程中的实际损耗,下列叙述错误的是( )
| A. | 消耗硫酸亚铁铵的物质的量为n(2-x)mol | |
| B. | 处理废水中Cr2O72-的物质的量为nx/2mol | |
| C. | 反应中发生转移的电子数为3nx NA | |
| D. | 在FeO•FeyCrxO3中,3x=y |
3.化学与日常生活紧密相关,下列说法错误的是( )
| A. | 氮肥NH4NO3在重力撞击下可能发生爆炸 | |
| B. | 在食品袋中放入盛有硅胶的透气小袋,可防止食物受潮 | |
| C. | 二氧化硅可用于制备太阳能电池板,晶体硅可用于制作光导纤维 | |
| D. | 碳酸氢钠可用来治疗胃酸过多 |

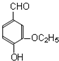 )是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基香草醛分子中两种含氧官能团的名称:酚羟基、醛基,核磁共振氢谱显示该分子中有7种不同类型的氢原子.
)是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基香草醛分子中两种含氧官能团的名称:酚羟基、醛基,核磁共振氢谱显示该分子中有7种不同类型的氢原子.
 ,属于取代反应(填反应类型).
,属于取代反应(填反应类型). .
. .
. )是一种医药中间体,请设计合理方案用茴香醛(
)是一种医药中间体,请设计合理方案用茴香醛( )合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).
)合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).
 .
.