题目内容
5.下列溶液中通入SO2时都会褪色,但二氧化硫的作用却可能不同.请分别再横线上写出在各变化中所体现的二氧化硫的性质:SO2通入酸性高锰酸钾溶液中红色褪去.还原性;SO2通入品红溶液红色褪去.漂白性;SO2通入溴水溶液中红棕色褪去.还原性;SO2通入氢氧化钠与酚酞的混合溶液红色褪去.酸性氧化物性质.
分析 依据二氧化硫为酸性氧化物,具有还原性、弱的氧化性、漂白性解答.
解答 解:二氧化硫具有还原性,SO2通入酸性高锰酸钾溶液,发生氧化还原反应使高锰酸钾红色褪去,体现二氧化硫还原性;二氧化硫具有漂白性,能够使品红溶液褪色;SO2通入溴水溶液中红棕色褪去是因为二氧化硫具有还原性,与溴水发生氧化还原反应,体现其还原性;二氧化硫为酸性氧化物能够与氢氧化钠反应生成亚硫酸钠和水,消耗氢氧根离子,所以溶液碱性减弱,红色退去,体现酸性氧化物的性质;
故答案为:还原性;漂白性;还原性;酸性氧化物性质.
点评 本题考查了物质的性质,熟悉二氧化硫具有的性质是解题关键,侧重考查学生对基础知识掌握熟练程度,题目难度不大.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
15.几种短周期元素的原子半径及主要化合价如表:
下列叙述正确的是( )
| 元素 | X | Y | Z | W |
| 原子半径/pm | 186 | 143 | 75 | 71 |
| 主要化合价 | +1 | +3 | +5、+3、-3 | -1 |
| A. | X、Y元素的金属性X<Y | |
| B. | Z的气态氢化物比W的气态氢化物稳定 | |
| C. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| D. | 四种元素对应的简单离子的离子半径大小顺序为Z3->W->X+>Y3+ |
16.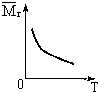 可逆反应2A+B?2C(g)△H<O,在一密闭容器中进行,随T(℃)变化容器中气体平均相对分子质量$\overline{M}$r的变化如图所示,则下列叙述中正确的是( )
可逆反应2A+B?2C(g)△H<O,在一密闭容器中进行,随T(℃)变化容器中气体平均相对分子质量$\overline{M}$r的变化如图所示,则下列叙述中正确的是( )
 可逆反应2A+B?2C(g)△H<O,在一密闭容器中进行,随T(℃)变化容器中气体平均相对分子质量$\overline{M}$r的变化如图所示,则下列叙述中正确的是( )
可逆反应2A+B?2C(g)△H<O,在一密闭容器中进行,随T(℃)变化容器中气体平均相对分子质量$\overline{M}$r的变化如图所示,则下列叙述中正确的是( )| A. | A和B可能都是固体 | |
| B. | A和B一定都是气体 | |
| C. | A和B可能都是气体 | |
| D. | 随温度的升高,容器中的压强一定在减小 |
13.除去NaCl中少量杂质CaCl2 Na2SO4,所用试剂及顺序正确的是( )
| A. | Na2CO3、BaCl2、HCl | B. | BaCl2、Na2CO3、HCl | ||
| C. | BaCl2、Na2CO3、HNO3 | D. | BaCl2、K2CO3、HNO3 |
20.在下列反应中,浓硫酸既表现强氧化性,又表现酸性的是( )
| A. | H2S+H2SO4(浓) | B. | Cu+H2SO4(浓) | C. | C+H2SO4 (浓) | D. | CuO+H2SO4 (浓) |
10.已知:H2S在与不足量的O2反应时,生成S和H2O.根据以下三个热化学方程式:
2H2S(g)+3O2(g)═2SO2(g)+2H2O(l)△H1
2H2S(g)+O2(g)═2S(s)+2H2O(l)△H2
2H2S(g)+O2(g)═2S(s)+2H2O(g)△H3
判断△H1、△H2、△H3三者大小关系正确的是( )
2H2S(g)+3O2(g)═2SO2(g)+2H2O(l)△H1
2H2S(g)+O2(g)═2S(s)+2H2O(l)△H2
2H2S(g)+O2(g)═2S(s)+2H2O(g)△H3
判断△H1、△H2、△H3三者大小关系正确的是( )
| A. | △H3>△H2>△H1 | B. | △H1>△H3>△H2 | C. | △H1>△H2>△H3 | D. | △H2>△H1>△H3 |
 烯烃A在一定条件下可以按如图的框图进行反应.
烯烃A在一定条件下可以按如图的框图进行反应.