题目内容
5.将铁粉和硫粉混合后加热,待反应一发生即停止加热,反应仍可持续进行,直至反应完全生成新物质.下列说法不正确的是( )| A. | 该反应是氧化还原反应 | |
| B. | 该反应的△H<0 | |
| C. | 生成新物质的化学式为 Fe2S3 | |
| D. | 生成新物质的总能量低于反应物铁粉和硫粉的总能量 |
分析 发生Fe+S$\frac{\underline{\;\;△\;\;}}{\;}$FeS,反应一发生即停止加热,反应仍可持续进行,可知该反应为放热反应,以此来解答.
解答 解:A.Fe、S元素的化合价变化,为氧化还原反应,故A正确;
B.为放热反应,则△H<0,故B正确;
C.S具有弱氧化性,反应生成FeS,故C错误;
D.为放热反应,则生成新物质的总能量低于反应物铁粉和硫粉的总能量,故D正确;
故选C.
点评 本题考查氧化还原反应及热效应,为高频考点,把握发生的反应及能量变化为解答的关键,侧重分析与应用能力的考查,注意S具有弱氧化性,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.硫代硫酸钠(Na2S2O3)与稀硫酸发生如下反应:Na2S2O3+H2SO4═Na2SO4+SO2+S↓+H2O下列四种情况中最早出现浑浊的是( )
| A. | 10℃时0.1 mol/L Na2S2O3和0.1 mol/L H2SO4各 5 mL | |
| B. | 20℃时0.1 mol/L Na2S2O3和0.1 mol/L H2SO4各 5 mL | |
| C. | 10℃时0.1 mol/L Na2S2O3和0.1 mol/L H2SO4各5 mL,加水10mL | |
| D. | 20℃时0.2mol/L Na2S2O3和0.1 mol/LH2SO4各5 mL,加水10 mL |
17.下列物质属于天然高分子化合物的是( )
| A. | 淀粉 | B. | 葡萄糖 | C. | 氨基酸 | D. | 油脂 |
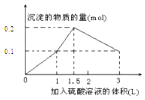
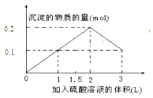
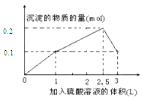
 用标签所示浓盐酸配制250mL 0.4mol/L的稀盐酸,并进行有关实验.请回答:
用标签所示浓盐酸配制250mL 0.4mol/L的稀盐酸,并进行有关实验.请回答: