题目内容
实验室里需要纯净的NaCl溶液,但手边只有混有Na2SO4、NH4HCO3的NaCl.某学生设计了如图所示方案提取纯净的NaCl溶液.(已知:NH4HCO3
NH3↑+CO2↑+H2O)
(1)150℃时,一定量的NH4HCO3完全分解后所得气体的平均相对分子质量为 .
(2)操作③所得到的悬浊液与胶体的本质区别是 .
(3)进行操作②后,判断SO42-是否已除尽方法是 .
(4)操作②加BaCl2溶液后生成沉淀,不必进行过滤就可进行操作③加碳酸钠溶液,其理由是 .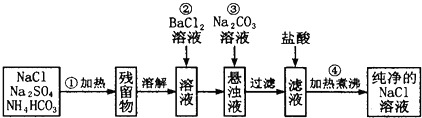
| ||
(1)150℃时,一定量的NH4HCO3完全分解后所得气体的平均相对分子质量为
(2)操作③所得到的悬浊液与胶体的本质区别是
(3)进行操作②后,判断SO42-是否已除尽方法是
(4)操作②加BaCl2溶液后生成沉淀,不必进行过滤就可进行操作③加碳酸钠溶液,其理由是

考点:粗盐提纯
专题:
分析:(1)根据碳酸氢铵受热分解产生氨气、水和二氧化碳,设碳酸氢铵的物质的量,利用摩尔质量在以g/mol为单位时,在数值上等于平均相对分子质量;
(2)悬浊液与胶体的本质区别是分散质微粒直径大小不同;
(3)加入氯化钡溶液看是否有白色沉淀来检验硫酸根离子是否除尽;
(4)制备试验中,过滤的次数少,可以减少溶质的损.
(2)悬浊液与胶体的本质区别是分散质微粒直径大小不同;
(3)加入氯化钡溶液看是否有白色沉淀来检验硫酸根离子是否除尽;
(4)制备试验中,过滤的次数少,可以减少溶质的损.
解答:
解:(1)设碳酸氢铵的物质的量为1mol,则
NH4HCO3
NH3↑+CO2↑+H2O
1mol 1mol 1mol 1mol
氨气、水和二氧化碳的质量分别为17g,44g,18g,在150℃时,水时气体,所以生成气体的平均摩尔质量M=
=26.3g/mol,相对分子质量26.3,
故答案为:26.3;
(2)悬浊液与胶体的本质区别是分散质微粒直径大小不同,故答案为:分散质微粒直径大小不同;
(3)加入过量氯化钡溶液除去硫酸根离子,检验硫酸根离子已除尽,可静止片刻在上层清液处,滴加一滴氯化钡溶液,不出现浑浊就说明硫酸根离子已经除尽,
故答案为:取少量上层澄清溶液,再滴加BaCl2溶液,如无沉淀出现则说明SO42-已除尽,反之则有(或其他的方法);
(4)操作②加BaCl2溶液后生成沉淀,不必进行过滤就可进行操作③加碳酸钠溶液,过滤的次数越少,可以减少溶质的损失,
故答案为:过滤的次数越少,越能减少溶质的损失.
NH4HCO3
| ||
1mol 1mol 1mol 1mol
氨气、水和二氧化碳的质量分别为17g,44g,18g,在150℃时,水时气体,所以生成气体的平均摩尔质量M=
| 17g+44g+18g |
| 3mol |
故答案为:26.3;
(2)悬浊液与胶体的本质区别是分散质微粒直径大小不同,故答案为:分散质微粒直径大小不同;
(3)加入过量氯化钡溶液除去硫酸根离子,检验硫酸根离子已除尽,可静止片刻在上层清液处,滴加一滴氯化钡溶液,不出现浑浊就说明硫酸根离子已经除尽,
故答案为:取少量上层澄清溶液,再滴加BaCl2溶液,如无沉淀出现则说明SO42-已除尽,反之则有(或其他的方法);
(4)操作②加BaCl2溶液后生成沉淀,不必进行过滤就可进行操作③加碳酸钠溶液,过滤的次数越少,可以减少溶质的损失,
故答案为:过滤的次数越少,越能减少溶质的损失.
点评:常见物质的分离方法和提纯是现在考试的重点和热点,可以根据所学知识进行回答,难度不大.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
室温下,石灰乳悬浊液存在下列平衡向Ca(OH)2(s)?Ca2+(aq)+2OH-(aq),此悬浊液中加入少量生石灰恢复至室温,下列说法中正确的是( )
| A、n(Ca2+)增大 |
| B、c(Ca2+)减小 |
| C、pH增大 |
| D、c(OH-)不变 |
下列家庭小实验不能制得溶液的是( )
A、 |
B、 |
C、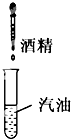 |
D、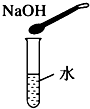 |
关于Cl-的说法正确的是( )
| A、Cl-呈黄绿色 |
| B、Cl-有毒 |
| C、Cl-具有17个电子 |
| D、Cl-是稳定结构 |
下列化学式所表示的物质一定是纯净物的是( )
| A、C3H8 |
| B、C4H8 |
| C、C2H6O |
| D、C7H8 |
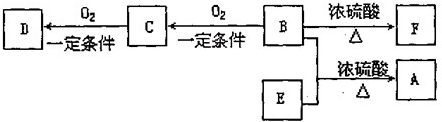
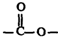 基团.
基团.