题目内容
下表是元素周期表的一部分,表中字母分别代表某一化学元素,请回答有关问题。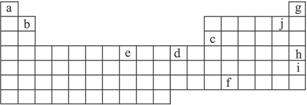
(1)人们曾认为g、h、i不发生化学反应,因而把它们叫做稀有气体,但是后来发现这族气体可以参加化学反应,你认为g、h、i中最有可能首先被发现可以参加化学反应的元素是_______________,其原因是_______________________________________________________。
(2)e是周期表中的_____________族元素,最外层电子数为_____________。
(3)a的阴离子半径_____________b的阳离子半径(填“大于”“等于”或“小于”)。
(4)在元素周期表中有一个对角线规则,其中包括b、c的化合物的性质十分相似。则b的氯化物与少量和过量的氢氧化钠溶液发生反应的离子方程式分别为(要表达出具体的元素符号,下同)__________________________________;______________________________。
(5)f的+4价氧化物可与浓盐酸反应,且已知其氧化性强于氯气,则该氧化物与浓盐酸反应的化学方程式可表示为____________________________________________________。
解析:解答此类题,首先要根据元素在周期表中的位置,确定其种类,然后根据元素周期律的知识加以回答。
答案:(1)i 从上到下,原子半径增大,失去电子越来越容易
(2)Ⅷ 2
(3)大于
(4) Be2++2OH-====Be(OH)2↓
Be2++4OH-====![]() +2H2O
+2H2O
(5)PbO2+4HCl====PbCl2+Cl2↑+2H2O

练习册系列答案
相关题目



 NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是
NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是 (4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是
(4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是