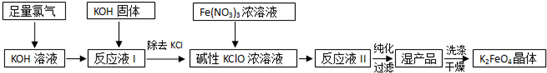
题目内容
9.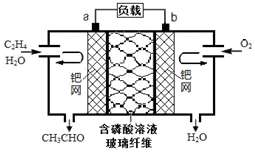 乙烯直接氧化法制乙醛的总反应方程式为2CH2═CH2+O2$\stackrel{PdCl_{2}•CuCl_{2}}{→}$2CH3CHO.下列有关说法正确的是( )
乙烯直接氧化法制乙醛的总反应方程式为2CH2═CH2+O2$\stackrel{PdCl_{2}•CuCl_{2}}{→}$2CH3CHO.下列有关说法正确的是( )| A. | 该电池可实现化学能与电能的相互转化 | |
| B. | 电子移动方向:电极a→磷酸溶液→电极b | |
| C. | 放电时,电路中每转移0.4mol电子,溶液中就有0.4molH+向负极迁移 | |
| D. | 该电池的负极反应式为:CH2═CH2-2e-+H2O=CH3CHO+2H+ |
分析 根据电池反应式知,该反应中O元素化合价由0价变为-2价而发生还原反应,所以通入氧气的电极是正极、通入乙烯的电极是负极,
A.该装置没有未接电源,所以不能将电能转化为化学能;
B.放电时,电子从负极沿导线流向正极;
C.原电池中阳离子向正极移动;
D、负极发生氧化反应,则负极电极方程式为CH2=CH2-2e-+H2O=CH3CHO+2H+.
解答 解:根据电池反应式知,该反应中O元素化合价由0价变为-2价而发生还原反应,所以通入氧气的电极是正极、通入乙烯的电极是负极,
A.该装置没有未接电源,所以不能将电能转化为化学能,所以不能实现化学能和电能的相互转化,故A错误;
B.放电时,电子从负极沿导线流向正极,通入乙烯的电极a是负极、通入氧化剂的电极b是正极,电子移动方向:电极a→负载→电极b,故B错误;
C.原电池中阳离子向正极移动,所以放电时,电路中每转移0.4mol电子,溶液中就有0.4molH+向正极迁移,故C错误;
D.负极发生氧化反应,所以负极电极方程式为CH2=CH2-2e-+H2O=CH3CHO+2H+,故D正确;
故选D.
点评 本题考查了原电池原理的应用,为高频考点,注意掌握电极方程式的书写是解决本题的关键,注意电子不能流经溶液,题目难度中等.

练习册系列答案
相关题目
19.下列措施或事实不能用勒夏特列原理解释的是( )
| A. | 工业合成氨生产中增大压强 | |
| B. | 在FeSO4溶液中加入少量铁粉以防止Fe2+被氧化 | |
| C. | NO2气体加压后颜色先变深再变浅 | |
| D. | 工业生产硫酸的过程中使用过量的空气以提高SO2的利用率 |
20.下列各情况下所含分子数目最多的是( )
| A. | 标态下 22.4 升氧气 | |
| B. | 常温常压下 66 克的 CO2 | |
| C. | 1.2mol 的硫酸 | |
| D. | 100ml,0.1mol•L-1 的氢氧化钠溶液 |
17.臭氧是理想的烟气脱硝试剂,其脱硝反应为:2NO2(g)+O3(g)?N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图象作出的判断正确的是( )
| A | B | C | D |
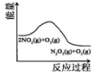 | 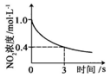 |  | 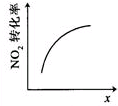 |
| 升高温度,平衡常数 减小 | 0~3s内,反应速率为v(NO2)=0.2mol•L-1•s-1 | t1时仅加入催化剂,平 衡向正方向移动 | 达平衡时,仅改变x, 则x为c(O2) |
| A. | A | B. | B | C. | C | D. | D |
4.NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 10 gH218O含有的中子数为5NA | |
| B. | 标准状况下,2.24LCH2Cl2含有的分子数为0.l NA | |
| C. | 1 mol氯气参加反应时,电子转移数目一定为2NA | |
| D. | 常温下,pH=6的纯水中OH-的数目为10-8NA |
14.据《俄新网》报道,萨彦斯克化工塑料厂一个生产二氯乙烷的高炉发生爆炸事故.该化工厂是俄罗斯一家最大的聚氯乙烯树脂生产厂家.下列有关二氯乙烷的说法不正确的是 ( )
| A. | 二氯乙烷与四氯乙烷的同分异构体数相同 | |
| B. | 在光照条件下,乙烷与氯气反应不能制备纯净的二氯乙烷 | |
| C. | 二氯乙烷和硝酸银溶液反应产生白色沉淀 | |
| D. | 二氯乙烷发生消去反应可以得到乙炔 |
3.在下列条件下,两种气体的分子数一定相等的是( )
| A. | 同密度、同压强的CO和C2H4 | B. | 同温度、同体积的O2和N2 | ||
| C. | 同体积、同密度的C2H4和N2 | D. | 同压强、同体积的O2和N2 |