��Ŀ����
 �������˻����ƻ�潫�й���ͳ�Ļ������˾����Լ��ִ��߿Ƽ���Ϊһ�壮��������ܴ����Դ�ڱ����ȼ�գ�������һ��������ȼ�ϣ��Իش��������⣺
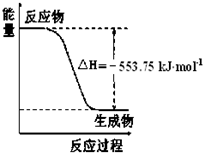
�������˻����ƻ�潫�й���ͳ�Ļ������˾����Լ��ִ��߿Ƽ���Ϊһ�壮��������ܴ����Դ�ڱ����ȼ�գ�������һ��������ȼ�ϣ��Իش��������⣺����ͼ��һ����������ȫȼ������CO2��1mol H2O��l�������е������仯ͼ����д����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ
�ڽ������Ѿ����Ƴ����飨C3H8��ȼ�ϵ�أ��õ�صĵ������ҺΪH2SO4��Һ��д���õ�ظ����ĵ缫��Ӧʽ��
��ij���������ԭ������Ϊ52.00����������ص��ý�����һ�ֺ������ε�����ˮ��Һʱ������ÿ�ų�2240mL����״�������壬������������ 10.4g���ڸú��������н����Ļ��ϼ�Ϊ
���㣺��Ӧ�Ⱥ��ʱ�,�Ȼ�ѧ����ʽ,������ѧ��Դ�����༰�乤��ԭ��
ר�⣺�����������������
�������ٷ���ͼ��õ�����1molˮ���ʱ��H=-553.75KJ/mol�������Ȼ�ѧ����ʽ��д����д����ע�����ʾۼ�״̬����Ӧ���µ��ʱ䣻
�ڱ���ȼ�ϵ�أ��õ�صĵ������ҺΪH2SO4��Һ��ȼ���ڸ���ʧ���ӷ���������Ӧ�������������õ����ӷ�����ԭ��Ӧ��ע��������ҺΪ����Һ�Ļ�����
�����ݵ������е缫��Ӧ�е���ת���غ㣬���������ͽ����ļ����ϵ�õ�����Ϊ��ص缫��Һ������·�е���ת���غ�õ��������ʵ��������Ħ����������������
�ڱ���ȼ�ϵ�أ��õ�صĵ������ҺΪH2SO4��Һ��ȼ���ڸ���ʧ���ӷ���������Ӧ�������������õ����ӷ�����ԭ��Ӧ��ע��������ҺΪ����Һ�Ļ�����
�����ݵ������е缫��Ӧ�е���ת���غ㣬���������ͽ����ļ����ϵ�õ�����Ϊ��ص缫��Һ������·�е���ת���غ�õ��������ʵ��������Ħ����������������
���
�⣺��ͼ����һ����������ȫȼ������CO2��1mol H2O��l�������е������仯ͼ����Ӧ���ȡ�H=-553.75KJ/mol����д�����Ȼ�ѧ����ʽΪ��
C3H8��g��+5O2��g��=3CO2��g��+4H2O��l������H1=-2215.0 kJ/mol��
�ʴ�Ϊ��C3H8��g��+5O2��g��=3CO2��g��+4H2O��l������H1=-2215.0 kJ/mol��
�ڱ���ȼ�ϵ�أ��õ�صĵ������ҺΪH2SO4��Һ��ȼ�ϱ����ڸ���ʧ���ӷ���������Ӧ���缫��ӦΪ��C3H8-20e-+6H2O=3CO2+20H+��
�ʴ�Ϊ��C3H8-20e-+6H2O=3CO2+20H+��
��ij���������ԭ������Ϊ52.00����������ص��ý�����һ�ֺ������ε�����ˮ��Һʱ������ÿ�ų� 2240ml����״�����������ʵ���=
=0.10mol�������������� 10.4g�����ʵ���=
=0.2mol�����ݵ����غ㣬��ϵ缫��Ӧ�õ�����������Ӧ��4OH--4e-=2H2O+O2���������缫��Ӧ��Mx++xe-=M�����ݵ����غ�õ���
xO2��4xe-��4M
x 4x 4
0.1mol 0.4mol 0.2mol
x=2��
���ݵ���ת���غ��֪��C3H8��g��+5O2��g��=3CO2��g��+4H2O��l����1molC3H8��g����Ӧ����ת��20mol��ת��0.4mol�������ı���Ϊ0.02mol����������ı��������=0.02mol��44g/mol=0.88g��
�ʴ�Ϊ��+2��0.88��
C3H8��g��+5O2��g��=3CO2��g��+4H2O��l������H1=-2215.0 kJ/mol��
�ʴ�Ϊ��C3H8��g��+5O2��g��=3CO2��g��+4H2O��l������H1=-2215.0 kJ/mol��
�ڱ���ȼ�ϵ�أ��õ�صĵ������ҺΪH2SO4��Һ��ȼ�ϱ����ڸ���ʧ���ӷ���������Ӧ���缫��ӦΪ��C3H8-20e-+6H2O=3CO2+20H+��
�ʴ�Ϊ��C3H8-20e-+6H2O=3CO2+20H+��
��ij���������ԭ������Ϊ52.00����������ص��ý�����һ�ֺ������ε�����ˮ��Һʱ������ÿ�ų� 2240ml����״�����������ʵ���=
| 2.24L |
| 22.4L?mol-1 |
| 10.4g |
| 52g?mol-1 |
xO2��4xe-��4M
x 4x 4
0.1mol 0.4mol 0.2mol
x=2��
���ݵ���ת���غ��֪��C3H8��g��+5O2��g��=3CO2��g��+4H2O��l����1molC3H8��g����Ӧ����ת��20mol��ת��0.4mol�������ı���Ϊ0.02mol����������ı��������=0.02mol��44g/mol=0.88g��
�ʴ�Ϊ��+2��0.88��
���������⿼�����Ȼ�ѧ����ʽ��֪ʶ�������Ȼ�ѧ����ʽ�ļ��㣬�缫ԭ���ĵ����غ�ļ���Ӧ�ã��缫��Ӧ��д�������缫��Ӧ����Ӧ���ǽ���ؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
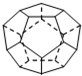 ��1���¹���������ѧ�������Ƴ���20��̼ԭ����ɵ� ������״����C20������״�ṹ��������������ι��� ����ͼ��ʾ������ش�C20���ӹ���
��1���¹���������ѧ�������Ƴ���20��̼ԭ����ɵ� ������״����C20������״�ṹ��������������ι��� ����ͼ��ʾ������ش�C20���ӹ��� �ķе��
�ķе�� �ߣ���ԭ����
�ߣ���ԭ���� ���ݻ�Ϊ1.00L�������У�ͨ��һ������N2O4��������ӦN2O4��g��?2NO2��g�������¶ȵ����ߣ�����������ɫ���
���ݻ�Ϊ1.00L�������У�ͨ��һ������N2O4��������ӦN2O4��g��?2NO2��g�������¶ȵ����ߣ�����������ɫ���
 ��һ�����Ϊ2L�ĺ����ܱ�������ͨ��2molX��g����1molY��g����������Ӧ��2X��g��+Y��g��?2Z��g������H��0
��һ�����Ϊ2L�ĺ����ܱ�������ͨ��2molX��g����1molY��g����������Ӧ��2X��g��+Y��g��?2Z��g������H��0