题目内容
17.常温下,在0.1mol/L的醋酸溶液中,水的离子积常数是( )| A. | 1×10-14 | B. | 1×10-13 | C. | 1×10-12 | D. | 1.32×10-14 |
分析 常温下水溶液中氢离子浓度和氢氧根离子浓度乘积为常数,为离子积常数,酸溶液中氢离子浓度大于氢氧根离子浓度;
解答 解:常温下水溶液中氢离子浓度和氢氧根离子浓度乘积为常数,离子积常数Kw=10-14,适用于稀酸、稀碱和盐溶液,常温下,在0.1mol/L的醋酸溶液中,水的离子积常数1×10-14,
故选A.
点评 本题考查了离子积常数的应用条件,离子积常数随温度变化,掌握基础是关键,题目较简单.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案
相关题目
7.下列分子中,含有σ键而不含π键的是( )
| A. | N2 | B. | Cl2 | C. | CH3CH3 | D. | C2H2 |
8.在Cu2S+2Cu2O═6Cu+SO2↑反应中,说法正确的是( )
| A. | Cu2O在反应中被氧化 | |
| B. | Cu2S在反应中既是氧化剂又是还原剂 | |
| C. | SO2是氧化产物 | |
| D. | 若反应中转移12mol电子,则生成6mol Cu |
5.化学与生产、生活、社会密切相关,下列说法错误的是( )
| A. | 绚丽缤纷的烟花中添加了含钾、钠、钙、铜等金属元素的单质或化合物 | |
| B. | 食用植物油的主要成分是高级脂肪酸甘油酯,是人体所需营养物质 | |
| C. | 臭氧、高锰酸钾溶液、次氯酸钠溶液、乙醇溶液均可用于消毒杀菌,且原理相同 | |
| D. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,与肺癌等疾病的发生相关 |
12.足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、NO的混合气体,这些气体与3.2g O2混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入NaOH溶液至Cu2+恰好完全沉淀,则消耗溶液中NaOH的质量是( )
| A. | 16 g | B. | 32 g | C. | 64 g | D. | 无法计算 |
2.下列关于胶体的叙述正确的是( )
| A. | Fe(OH)3胶体粒子直径在1nm~100 nm之间 | |
| B. | 胶体区别于其他分散系的本质特征是有丁达尔效应 | |
| C. | Fe(OH)3胶体中混有少量FeCl3,可以采取过滤的方法分离 | |
| D. | 将饱和FeCl3溶液滴加到沸水中长时间加热制得Fe(OH)3胶体 |
9.下列关于有机物的说法正确的是( )
| A. | 聚乙烯可发生加成反应 | |
| B. | 石油干馏可得到汽油、煤油等 | |
| C. | 丁烷的沸点低于丙醇 | |
| D. | 苯不能使酸性高锰酸钾溶液褪色,所以苯不能发生氧化反应 |
6.实验过程中要养成安全、规范、环保意识.下列说法正确的是( )
| A. | 浓碱飞溅到皮肤上,应立刻涂上硫酸溶液 | |
| B. | 金属钠着火,立刻用泡沫灭火器扑灭 | |
| C. | 加热试管时,先来回移动酒精灯加热,再对准药品集中加热 | |
| D. | 用天平称量固体药品时,砝码放在左盘 |
7.下列有关化学术语或物质变化的说法不正确的是( )
| A. | Na+的结构示意图为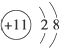 | |
| B. | 明矾的化学式为KAl(SO4)2•12H2O | |
| C. | 某微粒的电子数等于质子数,则该微粒可能是分子或离子 | |
| D. | 化学变化不产生新元素,产生新元素的变化不是化学变化 |