题目内容
3.用软锰矿(主要成分MnO2 )生产高锰酸钾产生的锰泥中,还含有18%的MnO2、3%的KOH(均为质量分数),及少量Cu、Pb的化合物等,用锰泥可回收制取MnCO3,过程如图所示: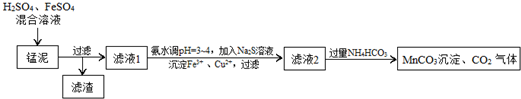
(1)高锰酸钾的氧化性强弱与溶液的酸碱性有关,在酸性条件下其氧化性较强.通常用来酸化高锰酸钾的酸是稀硫酸.
(2)除去滤液1中Cu2+ 的离子方程式是Cu2++S2-=CuS↓.
(3)经实验证明:MnO2稍过量时,起始H2SO4、FeSO4混合溶液中$\frac{c({H}^{+})}{c(F{e}^{2+})}$<0.7时,滤液1中能够检验出有Fe2+;$\frac{c({H}^{+})}{c(F{e}^{2+})}$≥0.7时,滤液1中不能检验出有Fe2+.根据上述信息回答①②③:
①检验Fe2+是否氧化完全的实验操作是取少量滤液1于试管中,加入铁氰化钾溶液,若无蓝色沉淀生成,证明Fe2+被氧化完全.
②生产时H2SO4、FeSO4混合溶液中$\frac{c({H}^{+})}{c(F{e}^{2+})}$应控制在0.7~1之间,不宜过大,请结合后续操作从节约药品的角度分析,原因是$\frac{c({H}^{+})}{c(F{e}^{2+})}$过大,在调节pH环节会多消耗氨水.
③若c(Fe2+)>1,调节c(Fe2+) 到0.7~1的最理想试剂是b(填序号).
a.NaOH溶液 b.铁粉 c.MnO
(4)写出滤液2中加入过量NH4HCO3反应的离子方程式Mn2++2HCO3-=MnCO3↓+CO2↑+H2O.
(5)上述过程锰回收率可达95%,若处理1740kg的锰泥,可生产MnCO3393.3kg.
分析 H2SO4、FeSO4混合溶液与锰泥中的二氧化锰发生氧化还原反应,将亚铁氧化为三价铁,然后过滤滤去未反应掉的二氧化锰和不溶的杂质,向滤液中氨水来调节溶液的PH值,并用硫化钠来沉淀铜离子和铅离子,然后过滤滤去生成的沉淀,最后向滤液中加入过量的碳酸氢铵生成碳酸锰,
(1)高锰酸钾溶液具有强氧化性,盐酸易被氧化生成氯气,一般用稀硫酸酸化;
(2)除去滤液1中Cu2+的是硫离子交换铜离子生成难溶于水的CuS;
(3)①检验Fe2+的存在加入铁氰化钾溶液,观察溶液是否变蓝;
②生产时H2SO4、FeSO4混合溶液中$\frac{c({H}^{+})}{c(F{e}^{2+})}$控制在0.7~1之间,不宜过大,如果比值越大说明硫酸的含量越高,后面用氨水调节PH时消耗的氨水的量多,造成原料的浪费;
③若$\frac{c({H}^{+})}{c(F{e}^{2+})}$>1,调节$\frac{c({H}^{+})}{c(F{e}^{2+})}$到0.7~1的方法是减小氢离子而增加亚铁离子的浓度,所以最好加入铁与氢离子发生氧化反应,生成氢气从而消耗氢离子,而生成亚铁离子;
(4)滤液2中的锰离子与NH4HCO3反应生成碳酸锰和二氧化碳与水;
(5)锰泥中含18%的MnO2,程锰回收率可达95%,根据关系式MnO2~~MnCO3,进行计算.
解答 解:H2SO4、FeSO4混合溶液与锰泥中的二氧化锰发生氧化还原反应,将亚铁氧化为三价铁,然后过滤滤去未反应掉的二氧化锰和不溶的杂质,向滤液中氨水来调节溶液的PH值,并用硫化钠来沉淀铜离子和铅离子,然后过滤滤去生成的沉淀,最后向滤液中加入过量的碳酸氢铵生成碳酸锰,
(1)高锰酸钾溶液具有强氧化性,盐酸易被氧化生成氯气,一般用稀硫酸酸化,
故答案为:稀硫酸;
(2)除去滤液1中Cu2+的是硫离子交换铜离子生成难溶于水的CuS,反应的离子方程式为:Cu2++S2-=CuS↓,
故答案为:Cu2++S2-=CuS↓;
(3)①检验Fe2+的存在加入铁氰化钾溶液,观察溶液是否变蓝,
故答案为:取少量滤液1于试管中,加入铁氰化钾溶液,若无蓝色沉淀生成,证明Fe2+被氧化完全;
②生产时H2SO4、FeSO4混合溶液中$\frac{c({H}^{+})}{c(F{e}^{2+})}$控制在0.7~1之间,不宜过大,如果比值越大说明硫酸的含量越高,后面用氨水调节PH时消耗的氨水的量多,造成原料的浪费,
故答案为:$\frac{c({H}^{+})}{c(F{e}^{2+})}$过大,在调节pH环节会多消耗氨水;
③若$\frac{c({H}^{+})}{c(F{e}^{2+})}$>1,调节$\frac{c({H}^{+})}{c(F{e}^{2+})}$到0.7~1的方法是减小氢离子而增加亚铁离子的浓度,所以最好加入铁与氢离子发生氧化反应,生成氢气从而消耗氢离子,而生成亚铁离子,向混合溶液中加适量铁粉,
故答案为:b;
(4)滤液2中的锰离子与NH4HCO3反应生成碳酸锰和二氧化碳与水,所以离子方程式为:Mn2++2HCO3-=MnCO3↓+CO2↑+H2O,
故答案为:Mn2++2HCO3-=MnCO3↓+CO2↑+H2O;
(5)锰泥中含18%的MnO2,程锰回收率可达95%,根据关系式
MnO2~~~~~~~~MnCO3,
87 115
1740kg×18%×95% m
解之得m=393.3kg,
故答案为:393.3.
点评 本题考查学生对元素及其化合物的主要性质的掌握、书写化学反应方程式、阅读题目获取新信息能力、对工艺流程的理解等,难度中等,需要学生具备扎实的基础与综合运用知识、信息分析解决问题能力.

| A. | AgNO3 | B. | CuSO4 | C. | NaOH | D. | NaCl |
| A. | 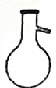 | B. |  | C. |  | D. | 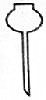 |
| A. | s电子云是球状,而p电子云是哑铃状 | |
| B. | 同一能层中,p能级上的电子比s能级上电子能量高 | |
| C. | 能量高的电子在离原子核较近的区域运动 | |
| D. | 各能级最多容纳电子数是该能级原子轨道数的两倍,其理论依据是泡利不相容原理 |
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42- HCO3- NO3- OH- |
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃片);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)将含1mol A的溶液与含1mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为Na2CO3.
(2)写出实验②发生反应的离子方程式:Al3++3OH-═Al(OH)3↓,Al(OH)3+OH-═[Al(OH)4]-.
(3)C常用作净水剂,用离子方程式表示其净水原理:Al3++3H2O?Al(OH)3(胶体)+3H+.
| A. | FeCl3 | B. | H2SO4 | C. | NaHCO3 | D. | Fe2S3 |

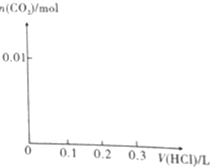 (1)将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol•L-1稀盐酸.在如图所示坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图象.
(1)将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol•L-1稀盐酸.在如图所示坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图象.