题目内容
下列说法正确的是( )
| A、在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实.2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g),则可推测该反应是吸热反应 | ||
B、室温下,将浓度为0.1mol?L?1HF溶液加水稀释,其电离平衡常数和
| ||
| C、电解精练铜时,阳极泥中常含有金属金、银、锌等 | ||
| D、锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后再用酸溶解去除 |
考点:吸热反应和放热反应,弱电解质在水溶液中的电离平衡,难溶电解质的溶解平衡及沉淀转化的本质,电解原理
专题:化学应用
分析:A.反应能否自发进行与反应条件无关;
B.HF属于弱电解质,则在加水不断稀释时,电离程度增大,电离平衡保持向正反应方向移动,并注意温度不变时,电离平衡常数不变;
C.粗铜中活泼性弱于铜的金属不放电沉淀在阳极底部形成阳极泥;
D.碳酸钙溶解度小于硫酸钙,从沉淀转化角度解答.
B.HF属于弱电解质,则在加水不断稀释时,电离程度增大,电离平衡保持向正反应方向移动,并注意温度不变时,电离平衡常数不变;
C.粗铜中活泼性弱于铜的金属不放电沉淀在阳极底部形成阳极泥;
D.碳酸钙溶解度小于硫酸钙,从沉淀转化角度解答.
解答:
解:A.反应能否自发进行可依据△H-T△S是否小于0判断,与反应的条件无关,故A错误;
B.因为因Ka(HF)=
,当HF溶液加水不断稀释,促进电离,c(F-)不断减小,温度不变,Ka(HF)不变,所以
增大,故B错误;
C.锌的活泼性强于铜,优先于铜放电,阳极泥中不可能含有锌,故C错误;
D.硫酸钙的溶解度大于碳酸钙,溶解度大的物质能向溶解度小的物质转化,故D正确;
故选:D.
B.因为因Ka(HF)=
| C(H+)C(F-) |
| C(HF) |
| c(H+) |
| c(HF) |
C.锌的活泼性强于铜,优先于铜放电,阳极泥中不可能含有锌,故C错误;
D.硫酸钙的溶解度大于碳酸钙,溶解度大的物质能向溶解度小的物质转化,故D正确;
故选:D.
点评:本题考查了反应的热效应,弱电解质电离平衡的移动,沉淀的转化,电极法精炼铜的原理,题目综合性强,难度中等,B选项为易错项,注意判断离子浓度变化时,可以借助于平衡常数表达式,运用整体法判断.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
下列实验操作不正确的是( )
| A、分液时,分液漏斗中上层液体应从漏斗口倒出 |
| B、蒸馏时,温度计水银球靠近蒸馏烧瓶支管口 |
| C、滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面 |
| D、蒸发时,当蒸发到剩有少量液体时,停止加热,利用余热将液体蒸干 |
化学与科技、生产、生活密切相关.下列说法不正确的是( )
| A、工业上,用焦炭在高温下还原二氧化硅制得粗硅 |
| B、“玉兔号”月球车太阳能电池帆板的材料是二氧化硅 |
| C、地沟油的主要成分是油脂,其组成与汽油、煤油不相同 |
| D、钠可把钛、锆、铌、钽等金属从它们的熔融的卤化物里还原出来 |
等质量的铁屑和锌粒与足量的同浓度的稀硫酸反应,下列图象可能正确的是( )
A、 |
B、 |
C、 |
D、 |
下列说法正确的是( )
| A、CH3CH2CH2CH3的二氯取代产物只有5种结构 |
| B、油脂的种类很多,但它们水解后都有一相同产物 |
| C、乙烯、苯、纤维素均属于烃类化合物 |
| D、苯和乙烯都能使溴水层褪色,均与溴水发生加成反应 |
短周期主族元素X、Y、Z、W的原子序数依次增大,X的原子半径比Y的小,X与W同主族,Y、Z族序数之和为11,Z原子最外层电子数是内层电子总数的3倍.下列说法不正确的是( )
| A、元素Z、W的简单离子的电子层结构相同 |
| B、元素Y的简单气态氢化物的热稳定性比Z的弱 |
| C、由X、Y、Z三种元素形成化合物,其水溶液可能显碱性 |
| D、W、Z两种元素形成的化合物中肯定不含共价键 |
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、标准状况下,0.56L丙烷中含有共价键的数目为0.2NA |
| B、常温常压下,6.4g氧气和臭氧中含有的分子总数为0.2NA |
| C、1mol羟基中电子数为10NA |
| D、0.1mol乙烯和乙醇的混合物完全燃烧所消耗的氧原子数一定为0.6NA |
下列实验过程和过程中涉及的离子反应方程式正确的是( )
| A、除去硫酸铜溶液中的硫酸亚铁以最终制备胆矾晶体:2Fe2++Cl2═2Fe3++2Cl- |
| B、Fe(OH)3与氢溴酸溶液混合:Fe(OH)3+3HBr═Fe3++3Br-+3H2O |
| C、用氨水吸收烟道气中的SO2:SO2+2NH3?H2O═2NH4++SO32-+H2O |
| D、醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
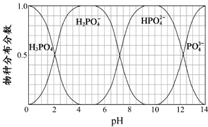 磷和砷是同主族的非金属元素.
磷和砷是同主族的非金属元素.