题目内容
14.取有机物3g,在足量的氧气中充分燃烧,将燃烧后的气体通过足量的浓硫酸,浓硫酸增重1.8g,将剩余气体通过足量澄清石灰水,得到10g 白色沉淀.求:(1)该有机物的最简式;
(2)取一定量该有机物,加热蒸发,测得该有机物蒸气密度为相同条件下氢气的15倍,试推测该有机物的分子式和结构简式.
分析 (1)浓硫酸增重1.8g,为水的质量,将剩余气体通过足量澄清石灰水,得到10g 白色沉淀,为碳酸钙的质量,可计算C、H的质量,进而计算3g有机物中O的质量,计算各元素的物质的量,可计算最简式;
(2)该有机物蒸气密度为相同条件下氢气的15倍,则相对分子质量为30,结合最简式可确定有机物分子式和结构简式.
解答 解:(1)n(H2O)=$\frac{1.8g}{18g/mol}$=0.1mol,m(H)=0.2g,n(C)=n(CaCO3)=$\frac{10g}{100g/mol}$=0.1mol,m(C)=0.1mol×12g/mol=1.2g,则m(O)=3g-1.2g-0.2g=1.6g,n(O)=$\frac{1.6g}{16g/mol}$=0.1mol,则n(C):n(H):n(O)=0.1:0.2:0.1=1:2:1,最简式为CH2O,
答:有机物的最简式为CH2O;
(2)该有机物蒸气密度为相同条件下氢气的15倍,则相对分子质量为30,则有机物分子式为CH2O,应为甲醛,结构简式为HCHO,
答:该有机物的分子式为CH2O,结构简式为HCHO.
点评 本题考查有机物的推断,为高频考点,侧重于学生的分析能力和计算能力的考查,注意掌握燃烧法利用原子守恒确定有机物分子式,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.为鉴定某盐成分,选用如图方法:下列结论正确的是( )
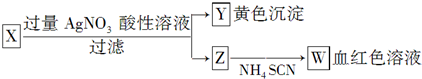

| A. | Z中一定有Fe3+ | B. | X中一定有Fe2+ | C. | Y为AgBr沉淀 | D. | X一定为FeBr2 |
2.下列气体不能用浓硫酸干燥的是( )
| A. | SO2 | B. | CO | C. | CO2 | D. | H2S |
9.关于苯的结构和性质叙述中,不正确的是( )
| A. | 苯可以用作有机溶剂 | |
| B. | 苯分子的结构简式可表示为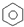 | |
| C. | 苯是单键与双键交替组成的环状结构 | |
| D. | 苯燃烧时能产生大量黑烟 |
6.下列各溶液中,微粒的物质的量浓度关系表述正确的是( )
| A. | 0.1 mol•L-1 Na2CO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-) | |
| B. | pH=12的Ba(OH)2溶液和pH=12的NaHCO3溶液中,水电离的c(H+)相等 | |
| C. | 将0.2 mol•L-1 NaA溶液和0.1 mol•L-1盐酸溶液等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-) | |
| D. | 常温下,pH=4的醋酸与pH=10的NaOH溶液等体积混合后c(OH-)<c(H+) |
3.表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )


| A. | 常压下五种元素的单质中,Z单质的沸点最高 | |
| B. | Y、Z的阴离子电子层结构都与R原子的相同 | |
| C. | 最高价氧化物对应的水化物的酸性W强于X | |
| D. | Y元素非金属性比W元素的非金属性强 |
4.同温同压下,等体积的两容器中分别充满NO和CO两种气体(其中N、C、O三种元素分别为14N、13C、18O),则下列说法正确的是( )
| A. | 两容器中分子间的平均距离不相同 | |
| B. | 两容器中所含微粒的质量均相同 | |
| C. | 两容器中所含原子数、分子数、中子数均相同 | |
| D. | 两容器中所含质子数、中子数均相同 |
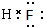 ;
;