题目内容
【题目】下列说法正确的是( )
A.PH=10的Mg(OH)2浊液C(Mg2+)=10﹣8 molL﹣1 (已知Mg(OH)2KSP=1×10﹣16)
B.已知AgClKSP=1.8×10﹣10;Ag2CrO4KSP=1.2×10﹣12则AgCl的溶解度一定比Ag2CrO4大
C.在饱和AgCl溶液中加入NaI固体不会发生变化
D.Fe3+在酸性溶液中一定不会生成Fe(OH)3沉淀
【答案】A
【解析】解:A、PH=10的Mg(OH)2浊液,c(OH﹣)=10﹣4mol/L,根据Ksp=c(Mg2+)c2(OH﹣),所以c(Mg2+)= ![]() =10﹣8 molL﹣1 , 故A正确; B、设AgCl溶解的浓度为xmol/L,则溶液中的银离子浓度为xmol/L,氯离子也为xmol/L,则根据溶度积为1.8×10﹣10=x×x,解得x=1.35×10﹣5mol/L
=10﹣8 molL﹣1 , 故A正确; B、设AgCl溶解的浓度为xmol/L,则溶液中的银离子浓度为xmol/L,氯离子也为xmol/L,则根据溶度积为1.8×10﹣10=x×x,解得x=1.35×10﹣5mol/L
同理设Ag2CrO4溶解的浓度为ymol/L,则溶液中的银离子浓度为2ymol/L,氯离子也为ymol/L,再根据溶度积为1.2×10﹣12=(2y)2×y,解得y=0.8×10﹣4mol/L,故溶解度较小的物质是AgCl,故溶度积小的溶解度反而大,所以Ksp的大小与溶解能力没有一定的关系,故B错误;
C、在饱和AgCl溶液中加入NaI固体,生成溶度积极小的黄色碘化银沉淀,故C错误;
D、铁离子在强酸性溶液中能稳定存在,弱酸性溶液中转化为氢氧化铁沉淀,故D错误;
故选A.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
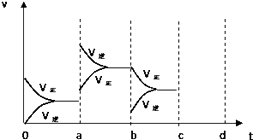
【题目】一定条件下反应A(g)+B(g)C(g)△H<0达到平衡后,据下列图象判断:
达到新的平衡对应的图象 | 平衡移动方向 | |
(i)使用催化剂 | ||
(ii)升温 | ||
(iii)降压 | ||
(iv)增加A的量 | ||
(v)减少C的量 |