题目内容
11.下列各变化中不属于原电池的反应的是( )| A. | 为防止轮船外壳生锈,在船底装上锌块 | |
| B. | 镀锌铁表面锌有划损时,也能阻止铁被氧化 | |
| C. | 在空气中金属铝表面迅速氧化形成保护层 | |
| D. | 锌和稀硫酸反应时,加入少量的CuSO4溶液可使反应加快 |
分析 属于原电池反应,说明符合原电池的构成条件,原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,与原电池无关说明不具备上述条件;
解答 解:A、铁、锌和电解质溶液符合原电池构成条件,则形成原电池,锌易失电子作负极,铁作正极,正极金属铁被保护,故A不符合;
B.铁、锌和电解质溶液符合原电池构成条件,则形成原电池,锌易失电子作负极,铁作正极,正极金属被保护,所以发生原电池反应,故B不符合;
C.在空气中,铝极易和氧气反应生成氧化物薄膜,该反应中没有两个活泼性不同的电极,不能构成原电池,所以发生的不是原电池反应,故C符合;
D.锌和稀硫酸反应时,加入少量的CuSO4溶液,锌置换铜,在稀硫酸溶液中形成原电池反应,可使反应速率加快,故D不符合;
故选C.
点评 本题考查了化学腐蚀和电化学腐蚀的判断,根据原电池构成条件来分析解答即可,难度不大.

练习册系列答案
相关题目
14.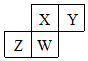 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )
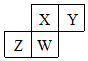 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )| A. | 原子半径:Z>W>X>Y | |
| B. | 元素X、Z的最高化合价分别与其主族序数相等 | |
| C. | 最高价氧化物对应水化物的酸性:Y>X>W | |
| D. | 最简单气态氢化物的热稳定性:Y>X>W>Z |
2.离子反应是一类重要反应,还原性Fe2+>Br-,下列有关离子方程式书写正确的是( )
| A. | 金属钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | Mg(OH)2与H2SO4反应:Mg2++2OH-+2H++SO42═MgSO4↓+2H2O | |
| C. | 向硫酸氢钠溶液加氢氧化钡溶液至完全沉淀:H++SO42-+OH-+Ba2+═BaSO4↓+H2O | |
| D. | FeBr2溶液与Cl2按照等物质的量反应:2Br-+Cl2═2Cl-+Br2 |
19.一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的( )
| A. | NaHSO4(固体) | B. | Na2SO4溶液 | C. | CuSO4(固体) | D. | NaCl(固体) |
6.一定物质的量浓度的NaCl、MgCl2、AlCl3三种溶液与同体积同浓度的AgNO3完全反应,消耗三溶液的体积比为3:2:1,则三种溶液中Cl-的物质的量浓度之比为( )
| A. | 1:1:1 | B. | 1:2:3 | C. | 3:2:1 | D. | 4:3:4 |
16.下列不能用于判断F 和 Cl的非金属性强弱的事实是( )
| A. | 气态氢化物的稳定性 | B. | 最高价氧化物对应的水化物的酸性 | ||
| C. | 单质与氢气反应的难易 | D. | F-和Cl-的还原性 |
20.在实验室中,对下来事故或药品的处理正确的是( )
| A. | 金属钠着火燃烧时,用泡沫灭火器灭火 | |
| B. | 未使用完的白磷要随时收集起来,并与空气隔绝 | |
| C. | 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 | |
| D. | 含硫酸的废液倒入水槽,用水冲入下水道 |
1.下列镁的化合物中,能与稀盐酸反应并生成无色有刺激性气味气体的是( )
| A. | MgO | B. | MgCO3 | C. | Mg2(OH)2CO3 | D. | Mg3N2 |
 如图是某硫酸试剂瓶标签上的内容:
如图是某硫酸试剂瓶标签上的内容: