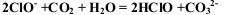题目内容
利用工厂的废铁屑(含少量Fe2O3、SiO2、锡等),制备绿矾(FeSO4·7H2O)的过程如下:

已知:①室温下饱和H2S溶液的pH约为3.9,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5。
②溶液X加KSCN不显红色。
(1)操作I的名称为 ,所需玻璃仪器为_______________。
(2)操作III的顺序依次为: 、冷却结晶、过滤、 、干燥。
(3)操作 II 中,试剂 Y 是_______,然后用稀硫酸将溶液酸化至 pH=2 的目的是 。
(4)写出绿矾与酸性高锰酸钾溶液反应的离子方程式 。
(5)常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至 pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过程中产品无损失。

上述实验①②③所用氢氧化钠均不含杂质,且实验数据可靠。通过计算,分析和比较上表3组数据,给出结论。
某酸性工业废水中含有K2Cr2O7。光照下,草酸H2C2O4能将其中的Cr2O72—转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始c(H+)和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表(表中不要留空格)。
实验编号 | 初始c(H+) | 废水样品体积/mL | 草酸溶液体积/mL | 蒸馏水体积/mL |
① | 1.0×10—4 | 60 | 10 | 30 |
② | 1.0×10—5 | 60 | 10 | 30 |
③ | 1.0×10—5 | 60 |
测得实验①和②溶液中的Cr2O72—浓度随时间变化关系如图所示。

(2)上述反应后草酸被氧化为 (填化学式)。
(3)实验①和②的结果表明 ;
实验①中0~t1时间段反应速率 (Cr3+)= mol·L—1·min—1 (用代数式表示)。
(Cr3+)= mol·L—1·min—1 (用代数式表示)。
(4)该课题组对铁明矾[Al2Fe(SO4)4·24H2O]中起催化作用的成分提出如下假设,请你完成假设二和假设三:
假设一: 起催化作用;假设二: ;假设三: ;
起催化作用;假设二: ;假设三: ;
(5)请你设计实验验证上述假设一,完成下表中内容。(除了上述实验提供的试剂外,可供选择的药品有K2SO4、FeSO4 、K2SO4·Al2(SO4)3·24H2O、Al2(SO4)3等。溶液中Cr2O72—的浓度可用仪器测定)
实验方案(不要求写具体操作过程) | 预期实验结果和结论 |



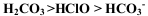 ,下列说法正确的是( )
,下列说法正确的是( )