题目内容
8.有人以化学反应:2Zn+O2+4H+═2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作.则原电池的负极材料是锌,发生的电极反应为Zn-2e-=Zn2+.分析 由反应2Zn+O2+4H+═2Zn2++2H2O可知,负极Zn失电子被氧化生成Zn2+.
解答 解:由反应2Zn+O2+4H+═2Zn2++2H2O可知,Zn失电子被氧化生成Zn2+,锌做负极,电极反应为Zn-2e-=Zn2+,
故答案为:锌;Zn-2e-=Zn2+.
点评 本题考查原电池的工作原理,为高频考点,侧重于学生分析能力的考查,注意把握原电池的工作原理以及电极反应,题目比较简单.

练习册系列答案
相关题目
18.一定质量的甲烷燃烧后的产物为CO、CO2和水蒸气,此混合气体质量为41.6g,当其缓慢经过无水CaCl2时,CaCl2增重21.6g.原混合气体中CO的质量为( )
| A. | 11.2g | B. | 13.2 g | C. | 8.8g | D. | 20g |
19.海洋中有丰富的食品、矿产、能源、药物和水产资源等(如图所示),

下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | 电解饱和的氯化钠溶液时阴极上产生的气体能使湿润的KI-淀粉试纸变蓝 | |
| B. | 第②步中结晶出的MgCl2•6H2O可在空气中受热分解制无水MgCl2 | |
| C. | 从第③步到第⑤步的目的是富集浓缩 | |
| D. | 在第③④⑤步中溴元素均被氧化 |
16.关于Na2O2+SO2=Na2SO4的说法正确的是( )
| A. | Na2O2做氧化剂 | B. | Na2O2做还原剂 | ||
| C. | Na2O2既做氧化剂又做还原剂 | D. | Na2O2既不做氧化剂又不做还原剂 |
3.在酸性溶液中能大量共存而且为无色、透明的溶液的一组是( )
| A. | NH4+、Al3+、SO42-、Fe2+ | B. | K+、Na+、NO3-、SO42- | ||
| C. | K+、MnO4-、NH4+、NO3- | D. | Na+、K+、HCO3-、NO3- |
13.没有做实验而欺骗老师的学生是( )
| A. | 老师,我用Na2SO3与BaCl2溶液作用,有白色沉淀生成,加入盐酸后沉淀消失 | |
| B. | 我向BaCl2溶液中通入SO2气体,也有白色沉淀生成 | |
| C. | 老师,我向Ba(OH)2溶液中通入SO2气体,也有白色沉淀生成老师 | |
| D. | 老师,我向用硝酸酸化的BaCl2溶液中通入SO2气体,我以为不会有沉淀,可出现了白色沉淀 |
20.共价键、离子键和范德华力是构成物质微粒间的不同作用力,下列物质中只含有上述一种作用力的是( )
| A. | 干冰 | B. | 氯化钠 | C. | 氢氧化钠 | D. | 冰 |
17.CuCl常用作有机合成催化剂,实验室以初级铜矿粉(主要含Cu2S及少量Fe2O3、FeO等)为原料制备活性CuCl.实验过程如图:
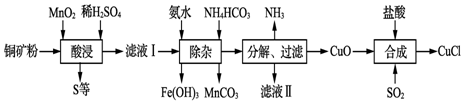
(1)“酸浸”中,加入稀H2SO4不宜过量太多的原因是避免“除杂”步骤消耗更多的氨水和NH4HCO3.
(2)已知:Cu(OH)2可溶于氨水形成深蓝色[Cu(NH3)4]2+溶液.
①“分解”实验条件及现象如表所示.
则“分解”实验条件应选C(填序号).
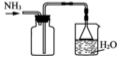
②“分解”生成的NH3可以回收利用.在实验室用图装置来收集NH3,当集气瓶收集满NH3时观察到的现象是漏斗中的液面忽上忽下.
(3)CuCl易氧化,Ksp(CuCl)=1.2×10-6.“合成”中生成CuCl的离子方程式为SO2+2CuO+2Cl-═2CuCl+SO42-;请补充从“合成”所得混合物中得到CuCl的实验操作步骤:过滤、洗涤、真空干燥或隔绝空气干燥
(4)请补充“除杂”步骤中分别回收Fe(OH)3和MnCO3的实验方案:向“滤液Ⅰ”中边搅拌边滴加氨水至溶液pH为[3.2,4.7),将所得沉淀过滤、洗涤、干燥得Fe(OH)3.再向滤液中边搅拌边滴加氨水和碳酸氢铵混合溶液至pH=10,有大量MnCO3沉淀生成,将沉淀过滤、洗涤、干燥得MnCO3.
【已知:pH=3.2时,Fe(OH)3沉淀完全;pH=4.7时,Cu(OH)2开始沉淀;pH=10时,MnCO3沉淀完全】

(1)“酸浸”中,加入稀H2SO4不宜过量太多的原因是避免“除杂”步骤消耗更多的氨水和NH4HCO3.
(2)已知:Cu(OH)2可溶于氨水形成深蓝色[Cu(NH3)4]2+溶液.
①“分解”实验条件及现象如表所示.
| 序号 | 温度/℃ | 压强/kPa | 时间/min | 残液颜色 |
| A | 110 | 101.3 | 60 | 浅蓝色 |
| B | 100 | 74.6 | 40 | 很浅 |
| C | 90 | 60.0 | 30 | 无色透明 |
②“分解”生成的NH3可以回收利用.在实验室用图装置来收集NH3,当集气瓶收集满NH3时观察到的现象是漏斗中的液面忽上忽下.

(3)CuCl易氧化,Ksp(CuCl)=1.2×10-6.“合成”中生成CuCl的离子方程式为SO2+2CuO+2Cl-═2CuCl+SO42-;请补充从“合成”所得混合物中得到CuCl的实验操作步骤:过滤、洗涤、真空干燥或隔绝空气干燥
(4)请补充“除杂”步骤中分别回收Fe(OH)3和MnCO3的实验方案:向“滤液Ⅰ”中边搅拌边滴加氨水至溶液pH为[3.2,4.7),将所得沉淀过滤、洗涤、干燥得Fe(OH)3.再向滤液中边搅拌边滴加氨水和碳酸氢铵混合溶液至pH=10,有大量MnCO3沉淀生成,将沉淀过滤、洗涤、干燥得MnCO3.
【已知:pH=3.2时,Fe(OH)3沉淀完全;pH=4.7时,Cu(OH)2开始沉淀;pH=10时,MnCO3沉淀完全】