题目内容
下列反应中,水作为还原剂的是( )
| A、2F2+2H2O═4HF+O2 |
| B、NaOH+HCl═NaCl+H2O |
| C、2Na+2H2O═2Na++2OH-+H2↑ |
| D、Cl2+H2O═HCl+HClO |
考点:氧化还原反应
专题:氧化还原反应专题
分析:水作为还原剂,则水中O元素的化合价升高,以此来解答.
解答:
解:A.F元素的化合价降低,水中O元素的化合价升高,则水为还原剂,故A选;
B.没有元素的化合价变化,不发生氧化还原反应,故B不选;
C.水中H元素的化合价降低,则水为氧化剂,故C不选;
D.只有Cl元素的化合价变化,水既不是氧化剂也不是还原剂,故D不选;
故选A.
B.没有元素的化合价变化,不发生氧化还原反应,故B不选;
C.水中H元素的化合价降低,则水为氧化剂,故C不选;
D.只有Cl元素的化合价变化,水既不是氧化剂也不是还原剂,故D不选;
故选A.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法正确的是( )
| A、在酸性条件下,CH3CO18OC2H5水解的产物是CH3CO18OH和C2H5OH |
| B、用甘氨酸(H2NCCH2COOH)和丙氨酸(CH3CHNH2COOH)缩合,最多可形成4种二肽 |
| C、C2H5Br与NaOH的乙醇溶液混合后加热,将所得气体通入高锰酸钾酸性溶液中,若溶液褪色,则证明有乙烯生成 |
| D、将电石与饱和食盐水反应生成的气体通入溴的四氯化碳溶液中,若溶液褪色,证明有乙炔生成 |
用NA表示阿伏伽德罗常数的值.下列判断正确的是( )
| A、2g H2含有的氢原子数目为NA |
| B、常温常压下,22.4L O2含有的分子数目为NA |
| C、1L 1mol?L-1 KOH溶液中含有的钾离子数目为NA |
| D、1mol Zn变为Zn2+时失去的电子数目为NA |
在主量子数为4的电子层中,能容纳的最多电子数是 ( )
| A、18 | B、24 | C、32 | D、36 |
某有机化合物的结构简式如图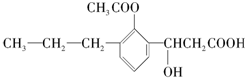 此有机化合物属于( )
此有机化合物属于( )
①烯烃 ②多官能团有机化合物 ③芳香烃 ④烃的衍生物 ⑤高分子化合物 ⑥酚类.
 此有机化合物属于( )
此有机化合物属于( )①烯烃 ②多官能团有机化合物 ③芳香烃 ④烃的衍生物 ⑤高分子化合物 ⑥酚类.
| A、①②③④ | B、②④ |
| C、②④⑤ | D、①③⑤⑥ |
下列实验操作中,仪器间不应该接触的是( )
| A、过滤时,漏斗下端管口与烧杯内壁 |
| B、使用胶头滴管时,尖嘴与试管内壁 |
| C、过滤时,盛被过滤液体的烧杯口与玻璃棒 |
| D、向试管倾倒液体药品时,试剂瓶口与试管口 |
扑热息痛是一种优良的解热镇痛剂,其结构式为 ,对此不正确的说法是( )
,对此不正确的说法是( )
 ,对此不正确的说法是( )
,对此不正确的说法是( )| A、该物质水解后不能得到α-氨基酸 |
| B、该物质与苯丙氨酸互为同分异构体 |
| C、该物质能与浓溴水发生取代反应 |
D、该物质可由 和CH3COOH经缩合而成 和CH3COOH经缩合而成 |
23gNa与过量O2反应生成Na2O和Na2O2的混合物,O2得到电子( )
| A、1mol |
| B、2mol |
| C、4mol |
| D、2mol~4mol之间 |



