题目内容
用NA表示阿伏伽德罗常数的值.下列判断正确的是( )
| A、2g H2含有的氢原子数目为NA |
| B、常温常压下,22.4L O2含有的分子数目为NA |
| C、1L 1mol?L-1 KOH溶液中含有的钾离子数目为NA |
| D、1mol Zn变为Zn2+时失去的电子数目为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.1个氢气分子含有2个氢原子;
B.常温常压下Vm≠22.4L/mol;
C.依据n=CV 计算氢氧化钾的物质的量,氢氧化钾为强电解质完全电离,依次计算钾离子数目;
D.1个Zn变为Zn2+时失去2个电子.
B.常温常压下Vm≠22.4L/mol;
C.依据n=CV 计算氢氧化钾的物质的量,氢氧化钾为强电解质完全电离,依次计算钾离子数目;
D.1个Zn变为Zn2+时失去2个电子.
解答:
解:A.1个氢气分子含有2个氢原子,2g H2的物质的量=
=1mol,含氢原子个数为2NA,故A错误;
B.常温常压下Vm≠22.4L/mol,22.4L O2的物质的量不是1mol,所以分子数不是NA,故B错误;
C.溶液中氢氧化钾的物质的量=1L×1mol?L-1 =1mol,氢氧化钾为强电解质完全电离,所以含钾离子的物质的量为1mol,个数为NA,故C正确;
D.1个Zn变为Zn2+时失去2个电子,1mol Zn变为Zn2+时失去的电子数目为2NA,故D错误;
故选:C.
| 2g |
| 2g/mol |
B.常温常压下Vm≠22.4L/mol,22.4L O2的物质的量不是1mol,所以分子数不是NA,故B错误;
C.溶液中氢氧化钾的物质的量=1L×1mol?L-1 =1mol,氢氧化钾为强电解质完全电离,所以含钾离子的物质的量为1mol,个数为NA,故C正确;
D.1个Zn变为Zn2+时失去2个电子,1mol Zn变为Zn2+时失去的电子数目为2NA,故D错误;
故选:C.
点评:本题考查阿伏加德罗常数的有关计算和判断,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,注意气体摩尔体积的使用条件.

练习册系列答案
相关题目
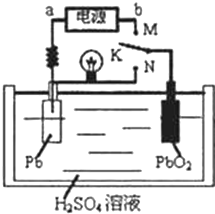 蓄电池属于二次电池.右图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液.电池反应为:Pb+PbO2+4H++2SO42-
蓄电池属于二次电池.右图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液.电池反应为:Pb+PbO2+4H++2SO42-| 放电 |
| 充电 |
下列有关说法正确的是( )
| A、实验室用铅蓄电池作电源电解饱和食盐水制取氯气,若制得氯气2.24L,则电池内消耗的H2SO4的物质的量是 0.2mol |
| B、K与N相接时,H+向正极区迁移 |
| C、K与M连接时,所用电源的b极为负极 |
| D、K与M相接时,阳极附近的pH逐渐增大 |
某反应的反应物与生成物有:K2Cr2O7、KCl、CrCl3、Cl2、HCl、H2O,已知氧化性K2Cr2O7>Cl2,则下列说法正确的是( )
| A、Cl2是该反应的还原产物 |
| B、氧化剂和还原剂的物质的量之比为1:1 |
| C、当转移0.2mol电子时,被氧化的还原剂的物质的量为0.2mol |
| D、由此反应可知还原性HCl<CrCl3 |
除去下列物质中的少量杂质(括号内为杂质),选用的试剂和分离方法均能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 乙烷(乙烯) | 氢气 | 催化剂、加热 |
| C | 四氯化碳(水) | / | 蒸馏 |
| D | 溴苯(Br2) | NaOH溶液 | 分液 |
| A、A | B、B | C、C | D、D |
设NA为阿佛加德罗常数,下列叙述正确的是( )
| A、通常状态下,O2与O3的混合物16克所含氧原子数为NA |
| B、将NO2和N2O4分子共NA个降温至标准状况下,其体积为22.4L |
| C、标况下,11.2LSO3所含的分子数目为0.5 NA |
| D、15.6gNa2O2跟过量CO2反应时,转移电子数为0.2NA |
下列各组物质中,互为同系物的是( )
A、CH3-CH=CH2和 |
B、 和 和 |
C、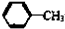 和 和 |
| D、CH2=CH-CH=CH2和CH3-CH2-CH2-C≡CH |
化合物A经李比希法和质谱法分析得知其相对分子质量为136,分子式C8H8O2.A分子中只含一个苯环且苯环上只有一个取代基,其核磁共振氢谱与红外光谱如图.关于A的下列说法中,不正确的是( )

| A、A属于酯类化合物,在一定条件下能发生水解反应 |
| B、A在一定条件下可与3mol H2发生加成反应 |
| C、符合题中A分子结构特征的有机物只有一种 |
| D、与A属于同类化合物的同分异构体只有2种 |
下列反应中,水作为还原剂的是( )
| A、2F2+2H2O═4HF+O2 |
| B、NaOH+HCl═NaCl+H2O |
| C、2Na+2H2O═2Na++2OH-+H2↑ |
| D、Cl2+H2O═HCl+HClO |
将适量的物质分别加到干燥的红色布条上,不能使其褪色的是( )
| A、新制的氯水 |
| B、氯化钙溶液 |
| C、液氯 |
| D、用盐酸酸化的次氯酸钠溶液 |