题目内容
6.以下氧化物既可以与酸反应,又可以与碱反应的是( )| A. | FeO | B. | Fe2O3 | C. | Al2O3 | D. | Fe3O4 |
分析 由两种元素组成且其中一种是氧元素的化合物是氧化物,既能与酸反应又能与碱反应的氧化物属于两性氧化物,据此分析解答.
解答 解:A、FeO只和酸反应不会和碱之间反应,故A错误;
B、Fe2O3只和酸反应不会和碱之间反应,故B错误;
C、Al2O3既可以与酸反应,又可以与碱反应,得到盐和水,属于两性氧化物,故C正确;
D、Fe3O4只和酸反应不会和碱之间反应,故D错误;
故选C.
点评 本题考查了基本概念的判断,明确两性氧化物、氧化物的概念即可解答,知道常见物质的性质,题目难度不大.

练习册系列答案
相关题目
16.下列有关NaHCO3与Na2CO3的说法中,正确的是( )
| A. | 分别加热两种样品,没有残留物质是NaHCO3 | |
| B. | 分别配成溶液,再加入石灰水,无白色沉淀生成的是NaHCO3 | |
| C. | 分别配成溶液,向其中逐滴加入同浓度的盐酸反应,先产生CO2的是NaHCO3 | |
| D. | 二者在一定条件下不能相互转化 |
14.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为3Zn+2K2FeO4+8H2O$?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
| A. | 充电时阳极反应为Zn-2e-+2OH-═Zn(OH)2 | |
| B. | 充电时OH-向阳极移动 | |
| C. | 放电时每转移3mole-正极有1molK2FeO4被氧化 | |
| D. | 充电时,电源的正极应与电池的Zn(OH)2极相连 |
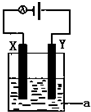
1.一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意图如图.下面对这种电池的说法正确的是( )


| A. | b极为电池的负极 | |
| B. | 当1mol乙醇被氧化转移12NA个电子 | |
| C. | 电池工作时电流由a极沿导线经灯泡再到b极 | |
| D. | 电池正极的电极反应为:O2+4e-+2H2O=4OH- |
18.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 使苯酚显紫色的溶液:NH4+、K+、SCN-、NO3- | |
| B. | 加入铝粉产生氢气的溶液:Na+、K+、NO3-、Cl- | |
| C. | 澄清透明的溶液中:SO42-、K+、Cu2+、Cl- | |
| D. | 由水电离出的c(H+)•c(OH-)=10-22的溶液:Fe2+、Na+、NO3-、SO42- |
 氮氧化合物是大气污染的重要因素.
氮氧化合物是大气污染的重要因素.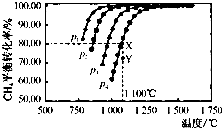
 (1)已知H-H 键能为436kJ•mol-1,H-N键键能为391kJ•mol-1,根据化学方程式:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1.则N≡N键的键能是945.6kJ•mol-1
(1)已知H-H 键能为436kJ•mol-1,H-N键键能为391kJ•mol-1,根据化学方程式:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1.则N≡N键的键能是945.6kJ•mol-1