题目内容
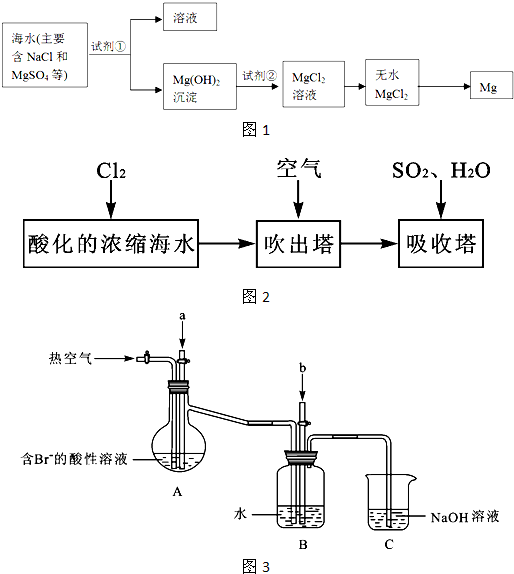
海洋约占地球表面积的71%,具有十分巨大的开发潜力.某校研究性学习小组同学对经初步净化处理的浓缩海水(主要含NaCl和MgSO4)进行研究.
(1)实验时若用托盘天平配制500mL0.20mol/LNaOH溶液,计算称量固体NaOH的质量.
(2)取初步净化处理的浓缩海水100mL,加入200mL0.20mol/LNaOH溶液,恰好把其中的Mg2+完全沉淀,则浓缩海水中Mg2+的物质的量浓度为多少?
(3)研究小组同学把上述沉淀完全转化为无水MgCl2,并在熔融状态下进行电解,可得标准状况下Cl2多少升?
(1)实验时若用托盘天平配制500mL0.20mol/LNaOH溶液,计算称量固体NaOH的质量.
(2)取初步净化处理的浓缩海水100mL,加入200mL0.20mol/LNaOH溶液,恰好把其中的Mg2+完全沉淀,则浓缩海水中Mg2+的物质的量浓度为多少?
(3)研究小组同学把上述沉淀完全转化为无水MgCl2,并在熔融状态下进行电解,可得标准状况下Cl2多少升?
分析:(1)根据NaOH溶液的物质的量浓度求出氢氧化钠的物质的量从而求出固体NaOH的质量;
(2)根据化学反应方程式求出氢氧化镁的物质的量从而求出浓缩海水中Mg2+的物质的量浓度;
(3)根据化学反应方程式求出氯气的物质的量从而求出氯气的体积.
(2)根据化学反应方程式求出氢氧化镁的物质的量从而求出浓缩海水中Mg2+的物质的量浓度;
(3)根据化学反应方程式求出氯气的物质的量从而求出氯气的体积.
解答:解:(1)氢氧化钠的物质的量n(NaOH)=C(NaOH)×V=0.20mol/L×0.5L=0.10mol,
固体NaOH的质量m(NaOH)=n(NaOH)?M(NaOH)═0.10mol×40g/mol=4.0g,
答:固体NaOH的质量为4.0g;
(2)设氢氧化镁的物质的量为x.
MgCl2 +2NaOH═Mg(OH)2↓+2NaCl
1 2
x 0.20L×0.20mol/L
=
x=0.02mol
所以c(Mg2+)=
=0.2mol/L
答:浓缩海水中Mg2+的物质的量浓度为0.2mol/L;
(3)设氯气的物质的量为y.
MgCl2(熔融)
Mg+Cl2↑
1 1
0.02mol y
=
y=0.02mol
V(Cl2)=0.02mol/L×0.1L×22.4L/mol=0.448L
答:可得标准状况下氯气0.448L.
固体NaOH的质量m(NaOH)=n(NaOH)?M(NaOH)═0.10mol×40g/mol=4.0g,
答:固体NaOH的质量为4.0g;
(2)设氢氧化镁的物质的量为x.
MgCl2 +2NaOH═Mg(OH)2↓+2NaCl
1 2
x 0.20L×0.20mol/L
| 1 |
| x |
| 2 |
| 0.20L×0.20mol/L |
x=0.02mol
所以c(Mg2+)=
| 0.02mol |
| 0.1L |
答:浓缩海水中Mg2+的物质的量浓度为0.2mol/L;
(3)设氯气的物质的量为y.
MgCl2(熔融)
| ||
1 1
0.02mol y
| 1 |
| 0.02mol |
| 1 |
| y |
y=0.02mol
V(Cl2)=0.02mol/L×0.1L×22.4L/mol=0.448L
答:可得标准状况下氯气0.448L.
点评:本题主要考查有关化学方程式的计算,难度不大,解题过程中首先要对反应原理搞清楚,其次要对根据方程式进行计算的步骤熟悉.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法错误的是( )
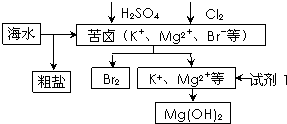

| A、可用BaCl2溶液除去粗盐中的SO42- | B、从苦卤中提取Br2的反应的离子方程式为:2Br-+Cl2═2Cl-+Br2 | C、试剂1可以选用石灰乳 | D、工业上,电解熔融MgO冶炼金属镁 |



 (2012?海淀区一模)海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法不正确的是( )
(2012?海淀区一模)海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法不正确的是( )