题目内容
下列与胶体有关的实验描述正确的是( )
| A、用一束激光照射胶体和溶液都有光亮的通路 |
| B、制备氢氧化铁胶体时加入的饱和氯化铁溶液越多越好 |
| C、用过滤的方法不能分离氢氧化铁胶体和氯化铁溶液 |
| D、向氢氧化铁胶体中加入过量盐酸后出现红褐色沉淀 |
考点:胶体的重要性质
专题:
分析:区分胶体的溶液可以利用丁达尔效应,胶体和溶液均能透过滤纸,胶体存在聚沉现象,据此判断选择即可.
解答:
解:丁达尔现象是胶体的特征性质,溶液没有,所以溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现明显光路,故A错误;
B、制备氢氧化铁胶体时加入的饱和氯化铁溶液应适量,故B错误;
C、用过滤的方法不能分离氢氧化铁胶体和氯化铁溶液,故C正确;
D、向氢氧化铁胶体中加入过量盐酸后先出现红褐色沉淀,后沉淀溶解,故D错误,故选C.
B、制备氢氧化铁胶体时加入的饱和氯化铁溶液应适量,故B错误;
C、用过滤的方法不能分离氢氧化铁胶体和氯化铁溶液,故C正确;
D、向氢氧化铁胶体中加入过量盐酸后先出现红褐色沉淀,后沉淀溶解,故D错误,故选C.
点评:本题考查了胶体和溶液的区别,胶体性质的应用,关键对胶体丁达尔效应的理解是解答的关键,题目难度不大.

练习册系列答案
相关题目
20g密度为dg/cm3的硝酸钙溶液中,含有1gCa2+离子,则NO3-离子的物质的量浓度为( )
A、
| ||
B、
| ||
| C、2.5dmol/L | ||
| D、1.25dmol/L |
某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下:
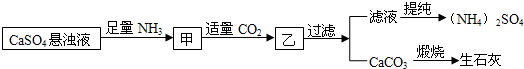
下列推断不合理的是( )

下列推断不合理的是( )
| A、生成1mol (NH4)2SO4至少消耗2mol NH3 |
| B、CO2可被循环使用 |
| C、先通二氧化碳,后通氨气,效果相同 |
| D、往甲中通CO2有利于制备(NH4)2SO4 |
下列各组物质间的反应既属于氧化还原反应,又属于离子反应的是( )
| A、Zn与稀H2SO4 |
| B、NaCl溶液与AgNO3溶液 |
| C、H2与O2 |
| D、Na2O与H2O |
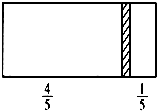 在一个密闭容器中,中间有一可自由滑动的隔板,将容器分成两部分.当左边充入1molN2,右边充入8gCO和CO2的混合气体时,隔板处于如图所示位置(两侧温度相同).则混合气体中CO和CO2的分子个数比为( )
在一个密闭容器中,中间有一可自由滑动的隔板,将容器分成两部分.当左边充入1molN2,右边充入8gCO和CO2的混合气体时,隔板处于如图所示位置(两侧温度相同).则混合气体中CO和CO2的分子个数比为( )| A、1:1 | B、1:3 |
| C、2:1 | D、3:1 |
下列说法正确的是(NA表示阿伏加德罗常数)( )
| A、在常温常压下,11.2LN2含有的分子数为0.5NA |
| B、在常温常压下,1molHe含有的原子数为NA |
| C、1mol H2O中含有2mol氢和1mol氧 |
| D、23g钠在化学反应中失去电子数目为10 NA |
下列物质的体积最大的是( )
| A、标况下,0.3 mol的NH3 |
| B、4℃时,18克水 |
| C、2mol的Al (密度为2.7g/cm3 ) |
| D、100g 37% 密度1.20 g/cm3 NaCl 溶液 |