题目内容
【题目】聚合硫酸铁可用于水的净化,化学式可表示为[Fea(OH)b(SO4)c]m,取其与足量盐酸反应,所得溶液平均分为两份,一份溶液加入足量的BaCl2溶液,得到沉淀4.66 g。另一份溶液,加入足量的NaOH溶液后过滤,对滤出固体洗涤,后灼烧得到红棕色固体质量为1.6 g,该聚合硫酸铁样品中a∶b的比值是
A. 1∶1B. 2∶1C. 3∶1D. 2∶5
【答案】A
【解析】
利用BaSO44.66g可以求出硫酸根的质量,利用Fe2O3质量为1.6g可以求出铁元素的质量,依据反应前后元素的质量不变可知该聚合物中硫酸根和铁元素的质量之比,从而可知a和c的比,而后利用化合物中元素的化合价代数和为零可求出b的值,据此解答。
4.66gBaSO4中含硫酸根的质量是4.66g×![]() =1.92g,1.6gFe2O3中铁的质量为1.6g×
=1.92g,1.6gFe2O3中铁的质量为1.6g×![]() =1.12g,由质量守恒定律可知该聚合物中硫酸根和铁元素的质量比是1.92:1.12=12:7,故由聚合物的化学式可知
=1.12g,由质量守恒定律可知该聚合物中硫酸根和铁元素的质量比是1.92:1.12=12:7,故由聚合物的化学式可知![]() ,则
,则![]() =1:1,令a=1,c=1,则由化合物中化合价的代数和为零可得3a-b-2c=0,则b=1,则该聚合硫酸铁样品中a:b的比值是1:1,故答案为A。
=1:1,令a=1,c=1,则由化合物中化合价的代数和为零可得3a-b-2c=0,则b=1,则该聚合硫酸铁样品中a:b的比值是1:1,故答案为A。

 快乐5加2金卷系列答案
快乐5加2金卷系列答案【题目】请参考题中图表,已知E1=134kJ/mol、E2=368kJ/mol,根据要求回答问题:
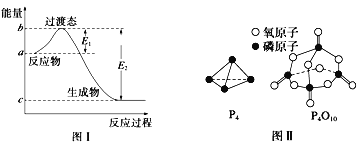
(1)图I是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能最变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是___(填“增大”、“减小”或“不变”下同),△H的变化是________。请写出NO2和CO反应的热化学方程式:__________。
(2)如表所示是部分化学键的键能参数:
化学键 | P-P | P-O | O=O | P=O |
键能/kJ/mol | a | b | c | x |
已知白磷的燃烧热为dkJ/mol,白磷及其完全燃烧的产物的结构如图II所示。1个P4O10分子中P-O的个数为_______,表中x=_____kJ/mol(用含a、b、c、d的代表数式表示)。
【题目】一定条件下,下列各组物质能一步实现图中所示转化关系的是

选项 | X | Y | Z | W |
A | Al | Al2O3 | NaAlO2 | Al(OH)3 |
B | Fe3O4 | Fe | FeCl2 | FeCl3 |
C | H2SO4 | SO2 | S | SO3 |
D | CH3CH2Br | CH2=CH2 | C2H5OH | CH2BrCH2Br |
A. A B. B C. C D. D
