题目内容
4.提纯下列物质(括号内少量杂质),所选用的除杂质试剂与分离方法正确的是( )| 不纯物质 | 处杂试剂 | 分离方法 | |
| A | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 分液 |
| B | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| C | 乙醇(水) | 新制生石灰 | 蒸馏 |
| D | 苯(苯酚) | 浓溴水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二者均与NaOH反应;
B.乙烯被高锰酸钾氧化生成二氧化碳;
C.CaO与水反应后,增大与乙醇的沸点差异;
D.溴、三溴苯酚均易溶于苯.
解答 解:A.二者均与NaOH反应,不能除杂,应利用饱和碳酸钠溶液、分液来除杂,故A错误;
B.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,应选溴水、洗气除杂,故B错误;
C.CaO与水反应后,增大与乙醇的沸点差异,然后蒸馏可除杂,故C正确;
D.溴、三溴苯酚均易溶于苯,不能除杂,应选NaOH、蒸馏除杂,故D错误;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离方法的选择为解答的关键,侧重分析与应用能力的考查,注意除杂的原则,题目难度不大.

练习册系列答案
相关题目
14.在通常条件下,下列各组物质的性质排列不正确的是( )
| A. | 沸点:乙烷>戊烷>2-甲基丁烷 | B. | 熔点:Al>Na>Na和K的合金 | ||
| C. | 密度:苯<水<1,1,2,2-四溴乙烷 | D. | 热稳定性:HF>HCl>H2S |
15.在下列反应中,HNO3既表现出氧化性,又表现出酸性的是( )
| A. | H2S+2HNO3=S↓+2NO2↑+2H2O | B. | Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O | ||
| C. | CuO+2HNO3=Cu(NO3)2+H2O | D. | 4HNO3$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+O2↑+2H2O |
12.关于铯(Cs)及其化合物的性质,说法正确的是( )
| A. | 金属铯的熔点比金属钠高 | B. | CsOH比NaOH的碱性强 | ||
| C. | Cs与H2O能剧烈反应,但没有钠剧烈 | D. | 碳酸铯难溶于水 |
19.常温常压下,某气态烃和氧气的混合气体20L,完全燃烧后通过浓硫酸后,再恢复到原来条件,气体体积变为原来的一半.设烃完全燃烧无剩余,则该烃可能是( )
①CH4 ②C2H4 ③C2H2 ④C2H6 ⑤C3H6 ⑥C3H4 ⑦C3H8 ⑧C4H6.
①CH4 ②C2H4 ③C2H2 ④C2H6 ⑤C3H6 ⑥C3H4 ⑦C3H8 ⑧C4H6.
| A. | 只有①③④ | B. | ⑤⑥⑦⑧ | C. | 只有②⑦ | D. | ①②④⑦ |
9.下列变化需克服相同类型作用力的是( )
| A. | 碘和干冰的升华 | B. | 硅和冰的熔化 | ||
| C. | 氯化氢和氯化钾的溶解 | D. | 氯化钠和冰融化 |
16.下列关于化学键的说法正确的是( )
| A. | 构成单质分子的微粒一定含有共价键 | |
| B. | 由非金属元素组成的化合物不一定是共价化合物 | |
| C. | 非极性键只存在于双原子分子中 | |
| D. | 含有共价键的化合物都是共价键化合物 |
1.在体积可变的密闭容器中,甲醇在浓硫酸的作用下发生如下反应:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-25kJ•mol-1,下列说法正确的是( )
| A. | 2mol甲醇参加反应,放出的热量为25kJ | |
| B. | 浓硫酸在反应中只作催化剂 | |
| C. | 2υ(CH3OH)=υ(CH3OCH3) | |
| D. | 升高温度或增大压强均可加快反应速率 |
 O2
O2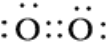 NH4+
NH4+ Na2O2
Na2O2
 CH4:
CH4: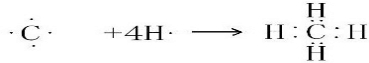 .
.