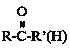题目内容
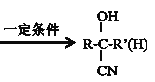
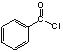
【题目】下列关于 的说法,不正确的是
的说法,不正确的是
A.在常温常压下,1mol 该物质与足量的 NaOH 溶液反应,最多消耗 1mol NaOH
B.该物质在一定条件下可以发生加聚反应
C.有机物的分子式为 C13H12O4Cl2
D.一定条件下,1mol 该物质能最多与 5mol 氢气加成
【答案】A
【解析】
A.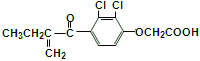 中含有羧基和Cl,能够与NaOH反应,在碱性条件下发生中和反应和水解反应,且水解生成的酚羟基也能与NaOH反应,则常温常压,1mol X与足量的NaOH溶液反应,最多可消耗5mol NaOH,故A错误;
中含有羧基和Cl,能够与NaOH反应,在碱性条件下发生中和反应和水解反应,且水解生成的酚羟基也能与NaOH反应,则常温常压,1mol X与足量的NaOH溶液反应,最多可消耗5mol NaOH,故A错误;
B.该物质中含有碳碳双键,在一定条件下可以发生加聚反应,故B正确;
C.根据结构简式,该有机物的分子式为 C13H12O4Cl2,故C正确;
D.能与氢气发生加成反应的有苯环、C=O键和碳碳双键,其中羧基中的C=O键不能反应,则1mol X与足量的氢气反应,最多消耗5mol H2,故D正确;
故选A。

【题目】请按要求回答下列问题:
(1)氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。已知:2C(s)+O2(g)=2CO(g)△H=-22lkJ/mol,
C(s)+O2(g)=CO2(g)△H=-393.5 kJ/mol,
N2(g)+O2(g)=2NO(g)△H=+181 kJ/mol,
则:2CO(g)+2NO(g)![]() N2(g)+2CO2(g)△H=__kJ/mol;
N2(g)+2CO2(g)△H=__kJ/mol;
下列措施能够增大此反应中NO的转化率的是___(填字母序号)
a.增大容器的体积 b.降低温度 c.增大CO的浓度 d.增大NO的浓度
(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g)△H=-574.5kJ/mol;NO和N2的物质的量变化如下表所示。
N2(g)+CO2(g)△H=-574.5kJ/mol;NO和N2的物质的量变化如下表所示。
物质的量/mol | T1/℃ | T2/℃ | |||||
0 | 5 min | 10 min | 15 min | 20 min | 25 min | 30 min | |
NO | 2.0 | 1.20 | 0.70 | 0.70 | 0.50 | 0.40 | 0.40 |
N2 | 0 | 0.40 | 0.65 | 0.65 | 0.75 | 0.80 | 0.80 |
①0~5min内,以NO表示的该反应速率υ(NO)=__________,该条件下的平衡常数K=___________(保留2位小数)。
②第15min后,温度调整到T2,数据变化如上表所示,则T1___________T2(填“>”、“<”或“=”)。
(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl-,利用Ag+与CrO42-生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-6mol·L-1)时,溶液中c(Ag+)为__mol·L-1,此时溶液中c(CrO42-)等于____mol·L-1。(已知Ksp(Ag2CrO4)=2.0×10-12,Ksp(AgCl)=2.0×10-10)。