题目内容
20.表是元素周期表的一部分,回答下列问题:周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | B | C | ||||||
| 3 | D | E | F | G | H | I | ||
(2)B元素的最高正化合价是+4.
(3)D、E、F三种元素的金属性逐渐减弱(填“减弱”或“增强”).
(4)某元素位于元素周期表中第3周期第VIA族,该元素的原子结构示意图是b(选填编号).
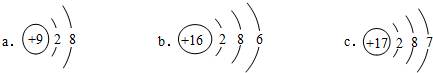
(5)化学键的断裂和形成都伴随着能量变化,那么1mol H2O→2mol H+1 mol O的变化过程要吸收(填“吸收”或“放出”)能量.
分析 由元素在周期表的位置可知,A为H,B为C,C为O,D为Na,E为Mg,F为Al,G为Si,H为S,I为Ar,
(1)稀有气体的性质最稳定;位于金属与非金属交界处的元素可作半导体材料;
(2)B为C,最外层电子数为4;
(3)同周期从左向右金属性减弱;
(4)元素位于元素周期表中第3周期第VIA族,可知原子结构中有3个电子层,最外层电子数为6;
(5)断裂化学键需要吸收能量.
解答 解:由元素在周期表的位置可知,A为H,B为C,C为O,D为Na,E为Mg,F为Al,G为Si,H为S,I为Ar,
(1)稀有气体的性质最稳定,则表中,最不活泼的元素是Ar;位于金属与非金属交界处的元素可作半导体材料,可用来制作半导体材料的物质的组成元素是Si,
故答案为:Ar;Si;
(2)B为C,最外层电子数为4,则最高正价为+4价,故答案为:+4;
(3)同周期从左向右金属性减弱,则D、E、F三种元素的金属性逐渐减弱,故答案为:减弱;
(4)元素位于元素周期表中第3周期第VIA族,可知原子结构中有3个电子层,最外层电子数为6,只有b符合,故答案为:b;
(5)断裂化学键需要吸收能量,则1mol H2O→2mol H+1 mol O的变化过程要吸收能量,故答案为:吸收.
点评 本题考查位置、结构与性质的关系,为高频考点,把握元素的位置和性质、元素周期律等为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
10.2013年2月朝鲜进行了第三次核试验,引起国际社会的极大关注.${\;}_{92}^{235}$U是一种重要的核燃料,这里的“235”是指该原子的( )
| A. | 质子数 | B. | 中子数 | C. | 质量数 | D. | 电子数 |
11.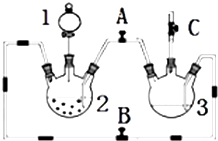 某化学兴趣小组拟用如图装置制备氢氧化亚铁并观察其颜色.提供化学药品:铁屑、稀硫酸、氢氧化钠溶液.
某化学兴趣小组拟用如图装置制备氢氧化亚铁并观察其颜色.提供化学药品:铁屑、稀硫酸、氢氧化钠溶液.
(1)稀硫酸应放在分液漏斗中(填写仪器名称).
(2)本实验通过控制A、B、C三个开关,将仪器中的空气排尽后,再关闭开关B、打开开关AC就可观察到氢氧化亚铁的颜色为白色.试分析实验开始时排尽装置中空气的理由防止生成的氢氧化亚铁被氧化.
(3)实验时为防止仪器2中铁粉通过导管进入仪器3中,可采取的措施是将铁粉换成铁块或铁钉.
(4)在FeSO4溶液中加入(NH4)2SO4固体可制备摩尔盐晶体[(NH4)2SO4•FeSO4•6H2O](相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇.
①为洗涤(NH4)2SO4•FeSO4•6H2O粗产品,下列方法中最合适的是D.
A.用冷水洗 B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗 D.用90%的乙醇溶液洗
②为了测定产品的纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol•L-1的酸性KMnO4溶液滴定.每次所取待测液体积均为25.00mL,实验结果记录如表:
滴定过程中发生反应的离子方程式为MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O.滴定终点的现象是最后一滴滴入,溶液由无色变为浅紫色,且30s不变色.
通过实验数据计算的该产品纯度为$\frac{980c}{a}$×100%(用字母ac表示).表中第一次实验中记录数据明显大于后两次,其原因可能是BC.
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低.
 某化学兴趣小组拟用如图装置制备氢氧化亚铁并观察其颜色.提供化学药品:铁屑、稀硫酸、氢氧化钠溶液.
某化学兴趣小组拟用如图装置制备氢氧化亚铁并观察其颜色.提供化学药品:铁屑、稀硫酸、氢氧化钠溶液.(1)稀硫酸应放在分液漏斗中(填写仪器名称).
(2)本实验通过控制A、B、C三个开关,将仪器中的空气排尽后,再关闭开关B、打开开关AC就可观察到氢氧化亚铁的颜色为白色.试分析实验开始时排尽装置中空气的理由防止生成的氢氧化亚铁被氧化.
(3)实验时为防止仪器2中铁粉通过导管进入仪器3中,可采取的措施是将铁粉换成铁块或铁钉.
(4)在FeSO4溶液中加入(NH4)2SO4固体可制备摩尔盐晶体[(NH4)2SO4•FeSO4•6H2O](相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇.
①为洗涤(NH4)2SO4•FeSO4•6H2O粗产品,下列方法中最合适的是D.
A.用冷水洗 B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗 D.用90%的乙醇溶液洗
②为了测定产品的纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol•L-1的酸性KMnO4溶液滴定.每次所取待测液体积均为25.00mL,实验结果记录如表:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
通过实验数据计算的该产品纯度为$\frac{980c}{a}$×100%(用字母ac表示).表中第一次实验中记录数据明显大于后两次,其原因可能是BC.
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低.
15.下列物质在通常条件下能与氢氧化钠溶液反应的是( )
| A. | 甲烷 | B. | 乙醇 | C. | 苯 | D. | 乙酸 |
5.某可充电的锂离子电池以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质.充放电时的电池反应为:Li+LiMn2O4$?_{充电}^{放电}$Li2Mn2O4.下列说法正确的是( )
| A. | 放电时,LiMn2O4发生氧化反应 | |
| B. | 放电时,正极反应为:Li++LiMn2O4+e-═Li2Mn2O4 | |
| C. | 充电时,LiMn2O4发生氧化反应 | |
| D. | 充电时,阳极反应为:Li++e-═Li |
12.关于下列物质的用途的说法错误的是( )
| A. | 部分卤代烃可用作灭火剂 | |
| B. | 甲醛的水溶液(福尔马林)可用于防腐 | |
| C. | 酚类化合物有毒,不能用于杀菌消毒 | |
| D. | 乙二醇可用于配制汽车防冻液 |
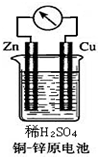 如图所示的铜-锌原电池中,
如图所示的铜-锌原电池中,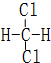 和
和 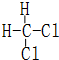 同一种物质.
同一种物质.