题目内容
物质的量浓度相同的下列溶液:
①Na2CO3 ②NaHCO3 ③H2CO3 ④(NH4)2CO3 ⑤NH4HCO3,
按c(CO32-)由小到大排顺序正确的是
- A.⑤<④<③<②<①
- B.③<⑤<②<④<①
- C.③<②<⑤<④<①
- D.③<⑤<④<②<①
B
碳酸属于弱酸,溶液的电离度很小,其他物质全部是强电解质,在溶液中全电离,所以碳酸溶液中c(CO32-)最小,Na2CO3和(NH4)2CO3溶液中直接可以电离出CO32所以c(CO32-)较大,但是在(NH4)2CO3溶液中铵根离子的水解会促进碳酸根的水解,使c(CO32-)减小,所以(NH4)2CO3溶液中c(CO32-)小于Na2CO3溶液中c(CO32-),NH4HCO3和NaHCO3会电离出碳酸氢根离子,然后再电离出碳酸根离子,但是铵根的水解会抑制碳酸氢根的电离,所以所以NH4HCO3溶液中c(CO32-)小于NaHCO3溶液中c(CO32-),综上所以答案选B。
碳酸属于弱酸,溶液的电离度很小,其他物质全部是强电解质,在溶液中全电离,所以碳酸溶液中c(CO32-)最小,Na2CO3和(NH4)2CO3溶液中直接可以电离出CO32所以c(CO32-)较大,但是在(NH4)2CO3溶液中铵根离子的水解会促进碳酸根的水解,使c(CO32-)减小,所以(NH4)2CO3溶液中c(CO32-)小于Na2CO3溶液中c(CO32-),NH4HCO3和NaHCO3会电离出碳酸氢根离子,然后再电离出碳酸根离子,但是铵根的水解会抑制碳酸氢根的电离,所以所以NH4HCO3溶液中c(CO32-)小于NaHCO3溶液中c(CO32-),综上所以答案选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
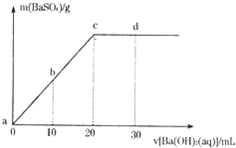 常温下,向0.1mol/L的H2SO4溶液中逐滴加入物质的量浓度相同的Ba(OH)2溶液,生成沉淀的质量和加入Ba(OH)2溶液的体积关系如下图所示,下列有关说法正确的是( )
常温下,向0.1mol/L的H2SO4溶液中逐滴加入物质的量浓度相同的Ba(OH)2溶液,生成沉淀的质量和加入Ba(OH)2溶液的体积关系如下图所示,下列有关说法正确的是( )| A、溶液的导电能力:a>b>c>d | B、溶液的pH:a<b<c<d | C、c点溶液和d点溶液均呈碱性 | D、b点溶液中c(H+)和d点溶液中c(OH-)相等 |