题目内容
11.下列有关聚乙烯的说法正确的是( )| A. | 聚乙烯是通过加聚反应生成的 | |
| B. | 聚乙烯具有固定的元素组成,因而具有固定的熔、沸点 | |
| C. | 聚乙烯塑料袋因有毒,不可以装食品 | |
| D. | 聚乙烯因性质稳定,故不易造成污染 |
分析 A.乙烯发生加聚反应生成聚乙烯;
B.聚合物的n值不确定;
C.聚乙烯塑料无毒,可用来生产食品袋、保鲜膜;
D.聚乙烯因性质稳定,不易分解.
解答 解:A.乙烯发生加聚反应生成聚乙烯,所以聚乙烯是乙烯的加聚反应后生成的高分子聚合物,故A正确;
B.聚合物的n值不确定,是混合物,没有固定的熔沸点,故B错误;
C.聚乙烯没有毒,可以用聚乙烯塑料袋装食品,而聚氯乙烯( )有毒,不能用于制作食品保鲜袋,故C错误;
)有毒,不能用于制作食品保鲜袋,故C错误;
D.聚乙烯因性质稳定,不易分解,造成白色污染,故D错误.
故选A.
点评 本题考查有机物的结构与性质,注意基础知识的积累,把握官能团与性质的关系为解答的关键,题目难度不大.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目
1.海洋资源的开发与利用具有广阔的前景.海水的pH一般在7.5~8.6之间.某地海水中主要离子的含量如表:
(1)海水显弱碱性的原因是(用离子方程式表示):HCO3-+H2O?H2CO3+OH-,该海水中Ca2+的物质的量浓度为5×10-3 mol/L.
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如如图1所示.其中阴(阳)离子交换膜只允许
阴(阳)离子通过.
①阴极的电极反应式为2H++2e-=H2↑.
②电解一段时间,阴极区会产生水垢,其成分为CaCO3和Mg(OH)2,写出生成CaCO3的离子方程式Ca2++OH-+HCO3-=CaCO3↓+H2O.
③淡水的出口为a、b、c中的b出口.
(3)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力.锂是制造化学电源的重要原料,如LiFePO4电池某电极的工
作原理如图2所示:
该电池的电解质是能传导 Li+的固体材料.
则放电时该电极是电池的正极(填“正”或“负”),电极反应式为FePO4+e-+Li+=LiFePO4.
(4)利用海洋资源可获得MnO2.MnO2可用来制备高锰酸钾:将MnO2与KOH混合后在空气中加热熔融,得到绿色的锰酸钾(K2MnO4),再利用氯气将锰酸钾氧化成高锰酸钾.该制备过程中消耗相同条件下空气和氯气的体积比为5:1(空气中氧气的体积分数按20%计).

| 成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | SO42- | HCO3- |
| 含量/mg?L-1 | 9360 | 83 | 200 | 1100 | 16000 | 1200 | 118 |
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如如图1所示.其中阴(阳)离子交换膜只允许
阴(阳)离子通过.
①阴极的电极反应式为2H++2e-=H2↑.
②电解一段时间,阴极区会产生水垢,其成分为CaCO3和Mg(OH)2,写出生成CaCO3的离子方程式Ca2++OH-+HCO3-=CaCO3↓+H2O.
③淡水的出口为a、b、c中的b出口.
(3)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力.锂是制造化学电源的重要原料,如LiFePO4电池某电极的工
作原理如图2所示:
该电池的电解质是能传导 Li+的固体材料.
则放电时该电极是电池的正极(填“正”或“负”),电极反应式为FePO4+e-+Li+=LiFePO4.
(4)利用海洋资源可获得MnO2.MnO2可用来制备高锰酸钾:将MnO2与KOH混合后在空气中加热熔融,得到绿色的锰酸钾(K2MnO4),再利用氯气将锰酸钾氧化成高锰酸钾.该制备过程中消耗相同条件下空气和氯气的体积比为5:1(空气中氧气的体积分数按20%计).

2.下列化合物既能通过单质间的化合反应制得,又能通过单质和稀盐酸反应制得的是( )
| A. | FeCl2 | B. | CuCl2 | C. | AlCl3 | D. | FeCl3 |
16.下列说法正确的是( )
| A. | 某次酸雨的pH为4.3,是由于溶解了CO2 | |
| B. | 生铁、不锈钢、青铜都属于合金 | |
| C. | 汽车尾气不会引起呼吸道疾病 | |
| D. | 普通玻璃的主要成分是纯碱、石灰石和石英 |
1.设NA为阿伏加德罗常数的值,下列说法一定正确的是( )
| A. | 25℃,pH=13的NaOH溶液中含有OH-为0.1NA | |
| B. | 一定条件下,4.6 g NO2和N2O4混合气体中含有的N原子数目为0.1NA | |
| C. | 标准状况下,22.4LH2O含有的分子数为1 NA | |
| D. | 78 g Na2O2与足量的H2O反应,电子转移个数为2NA |
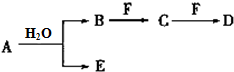 A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题:
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题: ;D中所含化学键的类型离子键、共价键.
;D中所含化学键的类型离子键、共价键.