题目内容
6.在一定条件下,Fe3O4+4CO=3Fe+4CO2反应中,四氧化三铁(填名称)是氧化剂,CO填化学式)发生氧化反应,C(填元素符号)元素被氧化,Fe(填化学式)是还原产物,生成42g Fe时转移的电子的物质的量是2mol.分析 Fe3O4+4CO═3Fe+4CO2反应中,Fe元素化合价降低,被还原,Fe3O4为氧化剂,C元素化合价升高,被氧化,CO为还原剂,以此解答.
解答 解:Fe3O4+4CO═3Fe+4CO2反应中,Fe元素化合价降低,被还原,四氧化三铁为氧化剂,C元素化合价升高,被氧化,CO为还原剂,Fe为还原产物,CO2为氧化产物,
生成42g Fe即$\frac{42g}{56g/mol}$=0.75mol时转移的电子的物质的量是2mol;
故答案为:Fe3O4;CO;C;Fe;2mol.
点评 本题考查氧化还原反应,为高频考点,侧重于学生的分析能力的考查,注意从元素化合价的角度认识相关概念和性质,难度不大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
16.下列反应的离子方程式正确的是( )
| A. | 碳酸钙溶于醋酸 CaCO3+2H+=Ca2++CO2↑+H2O | |
| B. | 氢氧化钠溶液吸收二氧化硫气体 SO2+2OHˉ=SO42ˉ+H2O | |
| C. | 氯气溶于水 Cl2+H2O═2H++Cl-+ClO- | |
| D. | 氯化铁溶液溶解铜 Cu+2Fe3+=Cu2++2Fe2+ |
17.在托盘天平的两盘中各放入一个质量相等的烧杯,两烧杯中各盛有100mL1mol/L 硫酸溶液,向两烧杯中分别加入各组中的两种物质,反应后天平保持平衡的是( )
| A. | 0.1mol Zn,0.1mol Fe | B. | 1mol Fe,1mol Zn | ||
| C. | 1g Zn,1g Fe | D. | 10g Zn,10g Fe |
14.将21.8g Na2O与Na2O2的混合物溶于足量水中,称得水溶液净重18.6g,则混合物中Na2O2和Na2O的质量之比为( )
| A. | 2:1 | B. | 78:31 | C. | 78:62 | D. | 39:62 |
1.与3.2gSO2所含的氧原子数相等的CO2的质量为( )
| A. | 2.2g | B. | 4.4g | C. | 44g | D. | 22g |
11.下列有关聚乙烯的说法正确的是( )
| A. | 聚乙烯是通过加聚反应生成的 | |
| B. | 聚乙烯具有固定的元素组成,因而具有固定的熔、沸点 | |
| C. | 聚乙烯塑料袋因有毒,不可以装食品 | |
| D. | 聚乙烯因性质稳定,故不易造成污染 |
18.下列化学用语不能正确表示相应粒子的是( )
| A. | C2H6的结构简式:CH3CH3 | B. | O2-的结构示意图: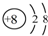 | ||
| C. | CO2的结构式:O=C=O | D. | HClO的电子式:H:Cl:O: |
15.下列分子式只能表示一种物质的是( )
| A. | C3H4Cl2 | B. | CH4O | C. | C2H6O | D. | C2H4O2 |
16.下列离子方程式正确的是( )
| A. | 铝片放入氢氧化钠溶液中:2Al+2H2O+2OH-═2AlO2-+3H2↑ | |
| B. | 钠与水反应:Na+2H2O═Na++OH-+H2↑ | |
| C. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| D. | 澄清石灰水与稀盐酸反应:Ca(OH)2+2H+═Ca2++2H2O |