题目内容
下列实验操作正确的是( )
| A、取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 |
| B、将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道 |
| C、制取NaCl晶体时,将蒸发皿中NaCl溶液全部加热蒸干 |
| D、用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,冷却至室温才能转移到容量瓶中 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.过量的药品应该回收处理,但Na、K除外;
B.实验后的废液应该回收处理;
C.将蒸发皿中NaCl溶液蒸至有很少量水时停止加热;
D.用氢气还原CuO原则是“先通氢后点灯,先熄灯后停氢”.
B.实验后的废液应该回收处理;
C.将蒸发皿中NaCl溶液蒸至有很少量水时停止加热;
D.用氢气还原CuO原则是“先通氢后点灯,先熄灯后停氢”.
解答:
解:A.用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为防止污染原溶液,应该将过量的试剂回收处理,不能倒入原试剂瓶中,故A错误;
B.硝酸钡属于重金属盐,随便丢弃对人或环境造成污染,所以其废液不能倒入下水道中,应该回收处理,故B错误;
C.将蒸发皿中NaCl溶液蒸至有很少量水时停止加热,利用余热将水分蒸干即可,故C错误;
D.用H2还原CuO的实验结束时,为防止反应后的Cu被氧化,应先停止加热,继续通H2直到试管冷却后再停止,故D正确;
故选D.
B.硝酸钡属于重金属盐,随便丢弃对人或环境造成污染,所以其废液不能倒入下水道中,应该回收处理,故B错误;
C.将蒸发皿中NaCl溶液蒸至有很少量水时停止加热,利用余热将水分蒸干即可,故C错误;
D.用H2还原CuO的实验结束时,为防止反应后的Cu被氧化,应先停止加热,继续通H2直到试管冷却后再停止,故D正确;
故选D.
点评:本题考查化学实验方案评价,侧重基本操作、实验原理考查,明确物质的性质及基本操作规范性即可解答,A为易错选项,一般的试剂如果量取过量时应该回收处理,因为Na、K极易和氧气、水反应而产生安全隐患,过量的K或Na应该放置在原瓶中,为易错点.

练习册系列答案
 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
化学概念在逻辑上存在如图关系,对下列概念的说法正确的是( )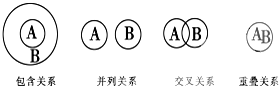

| A、化合物与电解质属于包含关系 |
| B、单质与非电解质属于包含关系 |
| C、溶液与分散系属于并列关系 |
| D、化合物与碱性氧化物属于交叉关系 |
反应4NH3+5O2?4NO+6H2O在一定体积的密闭容器中进行,30s后NO的物质的量浓度增加了3mol/L,则下列反应速率正确的是( )
| A、v (NO)=0.02 mol?(L?s)-1 |
| B、v (NO)=0.2mol?(L?s)-1 |
| C、v (NH3)=0.01 mol?(L?s)-1 |
| D、v (NH3)=0.1 mol?(L?s)-1 |
若将纳米碳均匀地分散到蒸馏水中,所形成的物质:①是溶液②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后析出黑色沉淀.其中正确的是( )
| A、①④⑥ | B、②③④ |
| C、②③⑤ | D、①③④⑥ |
关于△H的说法不正确的是( )
| A、反应的△H 由生成物与反应物的焓值差决定 |
| B、反应在恒压条件下的热效应为焓变 |
| C、某些反应的△H 可以通过实验测得 |
| D、放热反应的焓变取正值 |
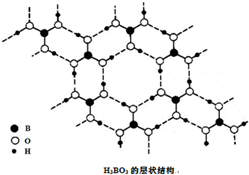 正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法正确的是( )
正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法正确的是( )| A、正硼酸晶体中只存在氢键 |
| B、H3BO3分子的稳定性与氢键有关 |
| C、分子中硼原子最外层为8电子稳定结构 |
| D、含1molH3BO3的晶体中有3mol氢键 |
关于丙烯醇(CH2=CH-CH2OH)的叙述不正确的是( )
| A、可使酸性高锰酸钾褪色,反应类型为氧化反应 |
| B、一定条件下可与氢气反应生成丙醇,反应类型为加成反应 |
| C、一定条件下能与乙酸反应生成酯,反应类型为酯化反应 |
| D、该物质与乙醇属于同系物 |