题目内容
某同学为了测定三聚氰胺的分子式,设计了如下实验:
查阅资料,三聚氰胺的相对分子质量为126,在常温下为晶体,由碳、氢、氮三种元素组成,加热条件下能与氧气发生反应生成二氧化碳、氮气和水.取12.6g三聚氰胺晶体按图示实验装置进行三聚氰胺与氧气的反应(假设三聚氰胺完全转化成产物),并通过测定生成物的量计算三聚氰胺的分子组成.
(1)写出A装置中发生反应的化学方程式 .
(2)C装置能不能与D装置互换? (填“能”或“不能”).理由是 .
(3)当B装置中反应完全发生后,读取F中水的体积的实验操作顺序为 (填序号).
①读数 ②冷却至室温 ③调平E、F装置中的液面
(4)测定数据如下:
经测定,E中收集的气体折合成标准状况下的体积为6.72L.
①利用上述实验数据,计算三聚氰胺的分子式为 .
②若B装置中没有铜网,对测定结果的影响是 .

查阅资料,三聚氰胺的相对分子质量为126,在常温下为晶体,由碳、氢、氮三种元素组成,加热条件下能与氧气发生反应生成二氧化碳、氮气和水.取12.6g三聚氰胺晶体按图示实验装置进行三聚氰胺与氧气的反应(假设三聚氰胺完全转化成产物),并通过测定生成物的量计算三聚氰胺的分子组成.
(1)写出A装置中发生反应的化学方程式
(2)C装置能不能与D装置互换?
(3)当B装置中反应完全发生后,读取F中水的体积的实验操作顺序为
①读数 ②冷却至室温 ③调平E、F装置中的液面
(4)测定数据如下:
| 装置 | C | D |
| 实验前 | 101.0g | 56.0g |
| 实验后 | 106.4g | 69.2g |
①利用上述实验数据,计算三聚氰胺的分子式为
②若B装置中没有铜网,对测定结果的影响是
考点:测定有机物分子的元素组成,有关有机物分子式确定的计算
专题:计算题,实验设计题
分析:(1)A应为在加热条件下制备氧气的装置,生成的氧气和与三聚氰胺发生反应;
(2)碱石灰既能吸收水,也能吸收二氧化碳,应分别测定水和二氧化碳的质量;
(3)读数时,气体的压强和外界大气压应相等;
(4)①先根据燃烧产物确定三聚氰胺晶体肯定含有C、H、N,可能含有O,然后根据C装置增重的质量为H2O,
D装置增重的质量为CO2,E中收集的6.72L气体为N2,求出C、H、N三种元素的质量,确定是否有O,求出实验式;
根据实验式和相对分子质量,求出分子式;
②炽热铜网可起到吸收氧气的作用.
(2)碱石灰既能吸收水,也能吸收二氧化碳,应分别测定水和二氧化碳的质量;
(3)读数时,气体的压强和外界大气压应相等;
(4)①先根据燃烧产物确定三聚氰胺晶体肯定含有C、H、N,可能含有O,然后根据C装置增重的质量为H2O,
D装置增重的质量为CO2,E中收集的6.72L气体为N2,求出C、H、N三种元素的质量,确定是否有O,求出实验式;
根据实验式和相对分子质量,求出分子式;
②炽热铜网可起到吸收氧气的作用.
解答:
解:(1)A应为在加热条件下制备氧气的装置,生成的氧气和与三聚氰胺发生反应,在加热条件下制备氧气的方法为氯酸钾和二氧化锰的反应或高锰酸钾分解反应,反应的方程式为,2KClO3
2KCl+3O2↑或2KMnO4
K2MnO4+MnO2+O2↑,
故答案为:2KClO3
2KCl+3O2↑或2KMnO4
K2MnO4+MnO2+O2↑;
(2)因碱石灰既能吸收H2O又能吸收CO2,若要分别测出H2O和CO2的质量,则先吸收H2O,后吸收CO2,浓硫酸吸水,碱石灰吸收二氧化碳,若互换位置,则碱石灰会同时吸收水和二氧化碳,导致实验失败,
故答案为:不能;浓硫酸吸水,碱石灰吸收二氧化碳,若互换位置,则碱石灰会同时吸收水和二氧化碳,导致实验失败;
(3)读数时,应待气体冷却至室温时,且将E、F两装置中的液面调平,以满足气体的压强和外界大气压应相等,故答案为:②③①;
(4)①H2O的质量为106.4g-101.0g=5.4g,物质的量为0.3mol,H的物质的量为0.6mol,H的质量为0.6g;CO2的质量为69.2g-56.0g=13.2g,物质的量为0.3mol,C的物质的量为0.3mol,C的质量为3.6g;N2的体积为6.72L,物质的量为0.3mol,N的物质的量为0.6mol,N的质量为8.4g;C、H、N三种元素的质量和为0.6g+3.6g+8.4g=12.6g,所以三聚氰胺晶体只有C、H、N三种元素,
N(C):N(H):N(N)=0.3mol:0.6mol:0.6mol=1:2:2,所以实验式为CN2H2,设分子式为(CN2H2)n,而三聚氰胺的相对分子质量为126,即42n=126,n=3,所以分子式为C3N6H6,
故答案为:C3N6H6;
②炽热铜网可起到吸收氧气的作用,若装置中没有铜网,则生成的氮气中含有氧气,故答案为:剩余氧气影响氮气体积的测定.
| ||
| △ |
| ||
故答案为:2KClO3
| ||
| △ |
| ||
(2)因碱石灰既能吸收H2O又能吸收CO2,若要分别测出H2O和CO2的质量,则先吸收H2O,后吸收CO2,浓硫酸吸水,碱石灰吸收二氧化碳,若互换位置,则碱石灰会同时吸收水和二氧化碳,导致实验失败,
故答案为:不能;浓硫酸吸水,碱石灰吸收二氧化碳,若互换位置,则碱石灰会同时吸收水和二氧化碳,导致实验失败;
(3)读数时,应待气体冷却至室温时,且将E、F两装置中的液面调平,以满足气体的压强和外界大气压应相等,故答案为:②③①;
(4)①H2O的质量为106.4g-101.0g=5.4g,物质的量为0.3mol,H的物质的量为0.6mol,H的质量为0.6g;CO2的质量为69.2g-56.0g=13.2g,物质的量为0.3mol,C的物质的量为0.3mol,C的质量为3.6g;N2的体积为6.72L,物质的量为0.3mol,N的物质的量为0.6mol,N的质量为8.4g;C、H、N三种元素的质量和为0.6g+3.6g+8.4g=12.6g,所以三聚氰胺晶体只有C、H、N三种元素,
N(C):N(H):N(N)=0.3mol:0.6mol:0.6mol=1:2:2,所以实验式为CN2H2,设分子式为(CN2H2)n,而三聚氰胺的相对分子质量为126,即42n=126,n=3,所以分子式为C3N6H6,
故答案为:C3N6H6;
②炽热铜网可起到吸收氧气的作用,若装置中没有铜网,则生成的氮气中含有氧气,故答案为:剩余氧气影响氮气体积的测定.
点评:本题主要考查了有机物分子式和结构简式的确定,侧重于学生的分析能力、实验能力和计算能力的考查,为高频考点,注意把握实验的原理以及计算方法,难度中等.

练习册系列答案
相关题目
和氖原子有相同的电子层结构的微粒是( )
| A、He |
| B、K+ |
| C、Cl- |
D、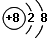 |
下列化学实验基本操作中,正确的是( )
| A、配制溶液时,将量筒中液体倒入烧杯后,应将量筒洗涤,将洗涤液也倒入烧杯 |
| B、用干燥的pH试纸分别测1mol?L-1的NaOH溶液和1mol?L-1的H2SO4的pH |
| C、稀释浓硫酸时,把浓硫酸慢慢倒入盛有水的烧杯中并不断搅拌 |
| D、向酒精灯加酒精时,应将试剂瓶中的酒精直接倒入酒精灯中 |
下列说法正确的是( )
| A、一定温度下,某溶液的pH<7,则该溶液呈酸性 |
| B、在水中加入少量碳酸钠固体将抑制水的电离 |
| C、0.02mol?L-1CH3COOH溶液和0.01mol?L-1NaOH溶液等体积混合,则溶液中:2c(H+)+c(CH3COOH)=2 c(OH-)+c(CH3COO-) |
| D、浓度均为0.1mol/L的NH4Cl溶液和NH4HSO4溶液,前者的c(NH4+)大于后者 |
下列有关电解质溶液中,说法正确的是( )
| A、0.2mol/L CH3COONa溶液和0.1mol/L HCl溶液等体积混合之后:c(Na+)=2c(Cl-)=c(CH3COO-)+c(CH3COOH)=0.2mol/L |
| B、0.1mol/LNa2CO3溶液:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| C、0.1mol/L的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
| D、25℃时,向10mL pH=4的盐酸中,加入pH=10的一元碱BOH溶液至pH刚好等于7,则反应后的溶液总体积:V总≤20mL |
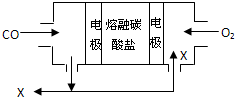 用熔融碳酸盐作电解质,CO、O2为原料组成的新型燃料电池如图所示,为了使该电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分X物质参与循环.下列说法错误的是( )
用熔融碳酸盐作电解质,CO、O2为原料组成的新型燃料电池如图所示,为了使该电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分X物质参与循环.下列说法错误的是( )| A、X物质的化学式为CO2 |
| B、通入O2的电极为正极 |
| C、负极的电极反应式为CO+CO32--2e-=2CO2 |
| D、电池工作时,转移0.5mol电子,理论上消耗O22.8L |
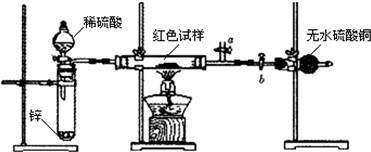 已知:①Cu2O与Cu均为红色固体,Cu2O酸性条件下易发生歧化反应.
已知:①Cu2O与Cu均为红色固体,Cu2O酸性条件下易发生歧化反应.