题目内容
下列物质中不属于离子化合物的是( )
| A、KCl |
| B、Ba(OH)2 |
| C、H2O |
| D、NH4Cl |
考点:离子化合物的结构特征与性质
专题:化学键与晶体结构
分析:含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,一般来说,活泼金属和活泼非金属元素之间易形成离子键.
解答:
解:A.KCl中钾离子和氯离子之间只存在离子键,为离子化合物,故A错误;
B.氢氧化钡中钡离子和氢氧根离子之间存在离子键、O原子和H原子之间存在共价键,为离子化合物,故B错误;
C.水分子中H原子和O原子之间存在共价键,为共价化合物,故C正确;
D.氯化铵中铵根离子和氯离子之间存在离子键、H原子和N原子之间存在共价键,为离子化合物,故D错误;
故选C.
B.氢氧化钡中钡离子和氢氧根离子之间存在离子键、O原子和H原子之间存在共价键,为离子化合物,故B错误;
C.水分子中H原子和O原子之间存在共价键,为共价化合物,故C正确;
D.氯化铵中铵根离子和氯离子之间存在离子键、H原子和N原子之间存在共价键,为离子化合物,故D错误;
故选C.
点评:本题考查了化合物和化学键的关系,明确基本概念是解本题关键,根据化合物中存在的化学键确定化合物类型,题目难度不大.

练习册系列答案
相关题目
研究物质变化时,人们可以从不同的角度、不同的层面来认识物质变化时所引起的化学键及能量变化.据此判断以下叙述中错误的是( )
| A、金属钠与氯气反应生成氯化钠后,稳定性增强,体系的能量降低 |
| B、物质燃烧可看成“储存”在物质内部的能量(化学能)转化为热能释放出来 |
| C、氮分子内部存在着很强的共价键,故通常状况下氮气的化学性质很不活泼 |
| D、需加热才能发生的反应一定是吸收能量的反应 |
下列能用勒沙特列原理解释的是( )
| A、加入催化剂后H2和O2反应生成水 |
| B、棕红色NO2加压后颜色先变深后变浅 |
| C、SO2催化氧化成SO3的反应,往往需要使用催化剂 |
| D、H2、I2、HI平衡混和气加压后颜色变深 |
 中草药素皮中含有的七叶树内酯 (碳氢原子未画出,每个折点表示一个碳原子),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别是( )
中草药素皮中含有的七叶树内酯 (碳氢原子未画出,每个折点表示一个碳原子),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别是( )| A、3 mol,2 mol |
| B、3 mol,4 mol |
| C、2 mol,3 mol |
| D、4 mol,4 mol |
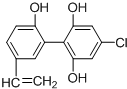 在2010年温哥华冬季奥运会上,有个别运动员因服用兴奋剂被取消参赛的资格.如图是检测出兴奋剂的某种同系物X的结构,关于X的说法正确的是( )
在2010年温哥华冬季奥运会上,有个别运动员因服用兴奋剂被取消参赛的资格.如图是检测出兴奋剂的某种同系物X的结构,关于X的说法正确的是( )| A、X分子中不可能所有原子都在同一平面上 |
| B、X遇到FeCl3溶液时显紫色,而且能使溴的四氯化碳溶液褪色 |
| C、1mol X与足量的浓溴水反应,最多消耗5mol Br2 |
| D、1mol X在一定条件下与足量的氢气反应,最多消耗1mol H2 |
下列说法不正确的是( )
| A、氨基酸是生命的基础,蛋白质是氨基酸的基石 |
| B、油脂碱性水解又称为皂化反应,因为油脂碱性水解后的产物为高级脂肪酸钠 |
| C、碘有“智力元素”之称,因为它是神经系统发育所不可缺少的 |
| D、维生素C药片的外面常包裹一层糖衣,因为维生素C具有还原性,易被氧化 |
 奥运会中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是( )
奥运会中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是( )| A、该物质与苯酚属于同系物 |
| B、该物质不能使酸性KMnO4溶液褪色 |
| C、1 mol该物质与浓溴水反应时最多消耗Br2为4 mol |
| D、该分子中的所有原子可能在同一平面 |
在一定条件下,RO3n-和I-发生如下反应:RO3n-+6I-+6H+═R-+3I2+3H2O(R为主族短周期元素),则下列关于R元素的说法中不正确的是( )
| A、RO3n-中R的化合价为+5价,n=1 |
| B、R位于元素周期表中的第VA族 |
| C、R的氢化物的水溶液和它的氧化物的水化物均呈酸性 |
| D、R的最外层电子为7 |
