题目内容
16.如图是常见四种有机物的比例模型示意图.下列说法正确的是( )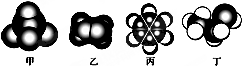
| A. | 甲的二氯代物只有一种 | |
| B. | 乙能与溴水发生取代反应而使溴水褪色 | |
| C. | 1mol丙中含有碳碳双键的数目是3NA | |
| D. | 丁在稀硫酸作用下可与甲酸发生取代反应 |
分析 由比例模型可知四种常见有机物分别为甲烷、乙烯、苯、乙醇,然后根据物质的性质分析.
A.甲烷为正四面体结构,所以其二氯代物只有1种;
B.乙烯中含双键,则与溴水发生加成反应使其褪色;
C.苯分子中不存在C-C及C=C键;
D.酯化反应需在浓硫酸作催化剂的条件下进行.
解答 解:由比例模型可知四种常见有机物分别为甲烷、乙烯、苯、乙醇,
A.甲烷为正四面体结构,甲烷中所有氢原子位置相同,所以其二氯代物只有1种,故A正确;
B.乙烯中含有碳碳双键,可与溴水发生加成反应而使溴水褪色,而不是发生取代反应而使溴水褪色,故B错误;
C.苯中不存在C-C及C=C键,碳键是介于碳碳单键和碳碳双键之间的独特的共价键,故C错误;
D.乙醇在浓硫酸作用下可与甲酸发生取代反应生成甲酸乙酯和水,故D错误;
故选A.
点评 本题主要考查了球棍模型、比例模型以及物质的性质,把握比例模型及对应化合物的性质为解答的关键,侧重常见几种烃和乙醇性质及结构的考查,题目难度不大,注意相关基础知识的积累.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
6.分子式为C5H10O2的羧酸共有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 种 |
4.下列有关实验说法错误的是( )
| A. | 在0.1mol/LK2Cr2O4溶液中,滴加3滴浓硫酸,K2Cr2O4溶液颜色会改变 | |
| B. | 在做温度对反应速率的影响实验时,应该将Na2S2O3和稀硫酸分别加热到设定温度再混合 | |
| C. | 恒温恒容已达H2(g)+I2(g)?2HI(g)平衡的容器中,充入少量HI(g),容器中气体颜色不变 | |
| D. | 不断读取数据,直到出现下降,取最大值,即为中和反应反应热的测定中混合溶液的最高温度 |
5.已知298K时,2SO2 (g)+O2(g)?2SO3(g);△H=-197kJ/mol,在相同温度和压强下,向某密闭容器中通人2mol SO2和1mol O2,达到平衡时放出热量Q1,向另一容积相同的密闭容器中通人1mol SO2和0.5mol O2,达到平衡时放出热量Q2,下列关系式正确的是( )
| A. | Q2 =$\frac{{Q}_{1}}{2}$ | B. | Q2 >$\frac{{Q}_{1}}{2}$ | C. | Q1 =Q2=197 kJ | D. | Q2 <$\frac{{Q}_{1}}{2}$<$\frac{197}{2}$kJ |
6.“类推”是一种常用的学习方法,但有时类推会产生错误的结论,下列类推结论中正确的是( )
| A. | NH4Cl加热分解只生成HCl和NH3,NH4I固体加热分解也只生成HI和NH3 | |
| B. | 第二周期元素氢化物的稳定性顺序是HF>H2O>NH3,则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 | |
| C. | 足量的CO2气体通入Na2SiO3中可生成NaHCO3; 足量的CO2气体通入石炭酸中也生成了NaHCO3 | |
| D. | 干冰(CO2)是分子晶体,则SiO2也是分子晶体 |
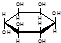 与葡萄糖
与葡萄糖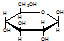 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物
的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物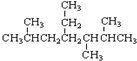 的名称为2,5,6-三甲基-4-乙基庚烷.
的名称为2,5,6-三甲基-4-乙基庚烷.