题目内容
某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及如图1所示装置制取NaHCO3,然后再将NaHCO3制成Na2CO3.

(1)装置丙中冷水的作用是 ;
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有 、洗涤、灼烧.NaHCO3转化为Na2CO3的化学方程式为 ;
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1min的NaHCO3样品的组成进行了以下探究.取加热了t1min的NaHCO3样品29.6g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中有关离子的物质的量的变化如图2所示.
则曲线a对应的溶液中的离子是 (填离子符号下同);曲线c对应的溶液中的离子是 ;该样品中NaHCO3和Na2CO3的物质的量之比是 ;
(4)若取21.0g NaHCO3固体,加热了t2 rnin后,剩余固体的质量为l4.8g.如果把此剩余固体全部加入到200mL 2mol?L-1的盐酸中,则充分反应后溶液中H+的物质的量浓度为 (设溶液体积变化忽略不计)

(1)装置丙中冷水的作用是
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1min的NaHCO3样品的组成进行了以下探究.取加热了t1min的NaHCO3样品29.6g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中有关离子的物质的量的变化如图2所示.
则曲线a对应的溶液中的离子是
(4)若取21.0g NaHCO3固体,加热了t2 rnin后,剩余固体的质量为l4.8g.如果把此剩余固体全部加入到200mL 2mol?L-1的盐酸中,则充分反应后溶液中H+的物质的量浓度为
考点:纯碱工业(侯氏制碱法)
专题:几种重要的金属及其化合物
分析:(1)温度越低,NaHCO3的溶解度越小;
(2)装置丙中是氨化的饱和食盐水中通入二氧化碳生成碳酸氢钠晶体,通过过滤得到晶体洗涤灼烧得到碳酸钠;NaHCO3转化为Na2CO3的方法是固体加热分解;
(3)混合物是碳酸钠和碳酸氢钠,滴入盐酸发生反应CO32-+H+=HCO3-; HCO3-+H+=CO2↑+H2O;依据图象分析碳酸根离子减小,碳酸氢根离子增多;
(4)依据反应前后质量变化是碳酸氢钠分解的原因,依据反应前后质量变化计算反应的碳酸氢钠和生成的碳酸钠,结合试样质量计算剩余碳酸氢钠,计算得到混合物反应消耗的氢离子得到.
(2)装置丙中是氨化的饱和食盐水中通入二氧化碳生成碳酸氢钠晶体,通过过滤得到晶体洗涤灼烧得到碳酸钠;NaHCO3转化为Na2CO3的方法是固体加热分解;
(3)混合物是碳酸钠和碳酸氢钠,滴入盐酸发生反应CO32-+H+=HCO3-; HCO3-+H+=CO2↑+H2O;依据图象分析碳酸根离子减小,碳酸氢根离子增多;
(4)依据反应前后质量变化是碳酸氢钠分解的原因,依据反应前后质量变化计算反应的碳酸氢钠和生成的碳酸钠,结合试样质量计算剩余碳酸氢钠,计算得到混合物反应消耗的氢离子得到.
解答:
解:(1)NaHCO3的溶解度随着温度的降低而减小,故用冷水可以使溶液冷却,降低NaHCO3的溶解度,使之更易析出,故答案为:冷却,使NaHCO3晶体析出;
(2)由装置丙中产生的NaHCO3发生的反应为,NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl;制取Na2CO3时需要过滤得到晶体,洗涤后加热灼烧得到碳酸钠;碳酸氢钠受热分解生成二氧化碳、碳酸钠、水,反应为:2NaHCO3
Na2CO3+H2O+CO2↑,
故答案为:过滤; 2NaHCO3
Na2CO3+H2O+CO2↑;
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1min的NaHCO3样品的组成进行了研究.取加热了t1min的NaHCO3样品29.6g 完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,发生反应 CO32-+H+=HCO3-; HCO3-+H+=CO2↑+H2O;溶液中有关离子的物质的量的变化为:碳酸根离子减小,碳酸氢根离子浓度增大,当碳酸根离子全部转化为碳酸氢根离子,再滴入盐酸和碳酸氢根离子反应生成二氧化碳,碳酸氢根离子减小,在此过程中,Na+不参与反应,浓度一直不变,故a曲线表示的是Na+浓度的变化;所以c曲线表示的是碳酸氢根离子浓度变化;碳酸根离子浓度0.2mol/L;碳酸氢根离子浓度为0.1mol/L;样品中NaHCO3和Na2CO3的物质的量之比是1:2;
故答案为:Na+;HCO3-;1:2;
(4)若取21g NaHCO3固体物质的量=
=0.25mol,加热了t1min后,剩余固体的质量为14.8g.
2NaHCO3=Na2CO3+CO2↑+H2O△m
2 1 62
0.2mol 0.1mol 21g-14.8g
反应后NaHCO3物质的量=0.25mol-0.2mol=0.05mol;NaHCO3+HCl=NaCl+H2O+CO2↑;消耗氯化氢物质的量0.05mol;
Na2CO3物质的量=0.1mol,Na2CO3+2HCl=2NaCl+H2O+CO2↑,消耗氯化氢物质的量0.2mol;剩余氯化氢物质的量=0.200L×2mol/L-0.05mol-0.2mol=0.15mol,剩余溶液中c(H+)=
=0.75mol/L,
故答案为:0.75mol/L.
(2)由装置丙中产生的NaHCO3发生的反应为,NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl;制取Na2CO3时需要过滤得到晶体,洗涤后加热灼烧得到碳酸钠;碳酸氢钠受热分解生成二氧化碳、碳酸钠、水,反应为:2NaHCO3
| ||
故答案为:过滤; 2NaHCO3
| ||
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1min的NaHCO3样品的组成进行了研究.取加热了t1min的NaHCO3样品29.6g 完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,发生反应 CO32-+H+=HCO3-; HCO3-+H+=CO2↑+H2O;溶液中有关离子的物质的量的变化为:碳酸根离子减小,碳酸氢根离子浓度增大,当碳酸根离子全部转化为碳酸氢根离子,再滴入盐酸和碳酸氢根离子反应生成二氧化碳,碳酸氢根离子减小,在此过程中,Na+不参与反应,浓度一直不变,故a曲线表示的是Na+浓度的变化;所以c曲线表示的是碳酸氢根离子浓度变化;碳酸根离子浓度0.2mol/L;碳酸氢根离子浓度为0.1mol/L;样品中NaHCO3和Na2CO3的物质的量之比是1:2;
故答案为:Na+;HCO3-;1:2;
(4)若取21g NaHCO3固体物质的量=
| 21g |
| 84g/mol |
2NaHCO3=Na2CO3+CO2↑+H2O△m
2 1 62
0.2mol 0.1mol 21g-14.8g
反应后NaHCO3物质的量=0.25mol-0.2mol=0.05mol;NaHCO3+HCl=NaCl+H2O+CO2↑;消耗氯化氢物质的量0.05mol;
Na2CO3物质的量=0.1mol,Na2CO3+2HCl=2NaCl+H2O+CO2↑,消耗氯化氢物质的量0.2mol;剩余氯化氢物质的量=0.200L×2mol/L-0.05mol-0.2mol=0.15mol,剩余溶液中c(H+)=
| 0.15mol |
| 0.2L |
故答案为:0.75mol/L.
点评:本题考查了工业制纯碱的原理分析,生产过程中的物质变化,混合物成分的分析判断和计算应用,实验过程分析,除杂操作,尾气吸收,图象定量分析判断,题目难度中等.

练习册系列答案
 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
下列关于化学用语的表示正确的是( )
A、碘化铵的电子式: |
B、间二甲苯的结构简式: |
| C、中子数为146、质子数为92的铀(U)原子:23892U |
D、氯原子的结构示意图: |
下列关于铝及其化合物的说法正确的是( )
| A、在常温下,浓硝酸不可储存在铝制容器中 |
| B、要从铝土矿中提取铝,必须获得较高纯度的氧化铝 |
| C、铝具有良好的抗腐蚀性,说明铝在空气中不易于氧气发生反应 |
| D、Al、Al2O3、AlCl3都既能和稀盐酸反应,又能和氢氧化钠溶液反应 |
某一有机物质的结构如下图所示.关于该物质的下列叙述中正确的是( )

| A、遇FeCl3溶液发生显色反应 |
| B、1mol该物质与3molNaOH恰好完全反应 |
| C、可发生氧化反应、酯化反应和消去反应 |
| D、该物质有3个苯环 |
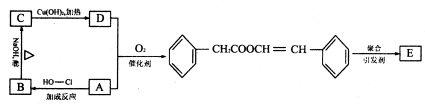
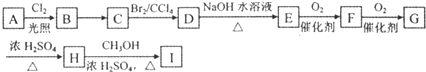

 的邻位异构体分子内脱水产物,香豆素的结构简式为
的邻位异构体分子内脱水产物,香豆素的结构简式为
 在一定条件下可水解为
在一定条件下可水解为 ;则F
;则F